Hepimiz Akraba mıyız? ALS, Genetik ve Ortak Atalarımızın Hikâyesi
Düşünsenize: Dünyadaki herkesle, çok ama çok uzak da olsa,
akraba olduğunuzu biliyor musunuz? Evet, hepimiz Afrika’dan yola çıkan
atalarımızın torunlarıyız! Peki, bu akrabalık bağı, genetik hastalıklarla nasıl
kesişiyor?
Özellikle ALS (Amiyotrofik Lateral Skleroz) gibi hem gizemli
hem de yıkıcı bir hastalık, genlerimizdeki ortak geçmişle nasıl bağlantılı?
Gelin, ALS’nin genetik dünyasına, göç yollarına, insanlık tarihinin çevresel
maceralarına ve ortak atalarımızın hikâyesine bir yolculuk yapalım.
ALS Nedir ve Neden
Önemli?
ALS, sinir hücrelerini etkileyen nadir ama ciddi bir
hastalık. Kasları kontrol eden motor nöronlar yavaş yavaş işlevini yitiriyor;
bu da yürüme, konuşma, hatta nefes alma gibi temel hareketlerin kaybına yol
açıyor. Çoğu insan ALS’yi, ünlü fizikçi Stephen Hawking’in yıllarca mücadele
ettiği hastalık olarak biliyor. Hawking, ALS ile uzun yıllar yaşadı, ama bu
hastalık genellikle 2-5 yıl içinde hayatı tehdit edebiliyor.
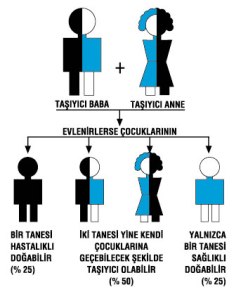
ALS’nin iki türü var: Genetik (ailesel) ve sporadik. Ailesel
ALS, vakaların %5-10’unu oluşturuyor ve genetik mutasyonlar anne-babadan çocuğa
geçiyor. Sporadik ALS ise daha yaygın (%90-95) ve genetik bir bağlantı olmadan,
“tesadüfi” gibi görünüyor. Ama işin ilginç yanı, sporadik ALS’de bile genetik
mutasyonlar rol oynayabiliyor! Yani, genlerimiz, bu hastalıkta sandığımızdan
daha büyük bir söz sahibi.
Genetik Mutasyonlar:
ALS’nin Gizli Şifreleri
ALS’nin genetik tarafı, bilim insanlarının en çok kafa
yorduğu alanlardan. Ailesel ALS’de en sık görülen mutasyonlar, SOD1, C9orf72,
TARDBP ve FUS genlerinde oluyor. Örneğin, C9orf72 mutasyonu, ALS vakalarının
%30-40’ında görülüyor ve özellikle Avrupa kökenli popülasyonlarda yaygın. Bu
mutasyon, DNA’da bir “tekrar dizisi” hatası yaratıyor ve sinir hücrelerini
yavaş yavaş zehirliyor.
Sporadik ALS’de ise mutasyonlar genellikle kalıtsal değil,
çevresel faktörler veya genetik hataların birikimiyle ortaya çıkıyor. Sporadik
olguların % 1-5’inde 21. kromozom üzerindeki Cu-Zn, Süperoksit Dismutaz (SOD1)
enziminin kodlandığı gen üzerinde mutasyon bulunmaktadır. Peki, bu mutasyonlar neden oluşuyor? Çevresel
toksinler, yaşam tarzı ya da genetik geçmişimizdeki başka faktörler mi
tetikleyici? İşte burada, insanlık tarihinin çevresel serüvenleri ve göç
yolları devreye giriyor.
Hepimiz Akrabayız: Göç Yolları ve Ortak Atalar
"Afrika'dan Çıkış" teorisine göre, yaklaşık
100.000 yıl önce, anatomik olarak modern insanlar (Homo sapiens) Afrika’dan
çıkıp dünyaya yayılmaya başladı. Bu büyük göç, genetik mirasımızın temelini
attı. Genetik çalışmalar, hepimizin “Mitokondriyal Havva” ve “Y-kromozomal Âdem”
denen ortak atalardan geldiğini gösteriyor. Tabii bu, tek bir anne-baba çifti
demek değil; binlerce yıl önceki genetik havuzun temsilcileri bunlar.
 |
Şekil 1 NordNordWest - Spreading homo sapiens ru.svg by Urutseg which based on Spreading homo sapiens.jpg by Altaileopard, Kamu Malı, https://commons.wikimedia.org/w/index.php?curid=34697001 |
İnsan Genom Projesi veya (1000 Genom Projesi), tüm insanların ortak atalardan geldiğini ve genetik olarak %99,9 oranında benzer olduğumuzu ortaya koydu.
Göç yolları, genetik çeşitliliğimizi şekillendirdi.
Avrupa’ya, Asya’ya, Amerika’ya, Avustralya’ya yayılan insanlar, farklı
coğrafyalarda genetik havuzlar oluşturdu. Ama bazı bölgelerde, örneğin izole
ada topluluklarında veya akraba evliliklerinin yaygın olduğu yerlerde, genetik
havuz daraldı. Bu, bazı genetik hastalıkların belirli bölgelerde sık
görülmesine neden oldu. Talasemi, Akdeniz ülkelerinde sık görülüyor ve akraba
evlilikleri bu hastalığın prevalansını artırıyor. Tay-Sachs hastalığı, belirli
etnik gruplarda (ör. Aşkenazi Yahudileri) daha yaygın. ALS için de bu geçerli.
Örneğin, C9orf72 mutasyonu Avrupa’da, özellikle İskandinav ülkelerinde yaygın.
Bunun nedeni, bu mutasyonun binlerce yıl önceki bir ortak atadan yayılmış
olması olabilir. Asya’da ise SOD1 mutasyonları daha sık; Japonya ve Çin’de ALS
hastalarında bu genetik değişiklikler öne çıkıyor. Bu farklılıklar, insanlık
tarihinin göç haritasıyla örtüşüyor. İpek Yolu, kolonyal dönem ve modern
göçler, genlerin karışmasını sağladı ama bazı mutasyonlar belirli bölgelerde
“kök saldı”.
Salgınlar, Radyasyon
ve Epigenetik: Genetik Havuzumuzu Şekillendiren Görünmez Eller
İnsanlık tarihi, sadece göçlerle değil, salgınlar, viral
enfeksiyonlar, radyoaktivite, kozmik ışınlar ve epigenetik faktörler gibi
çevresel faktörlerle da şekillendi. Örneğin, veba, grip pandemileri veya çiçek
hastalığı gibi salgınlar, insan popülasyonlarını azalttı ve genetik havuzda iz
bıraktı. Bazı virüsler, DNA’mıza entegre olarak nesiller boyu taşındı; bu, ALS
gibi hastalıklarda rol oynayan mutasyonların kökeni olabilir. Doğal radyoaktivite, özellikle 20. yüzyıldaki
nükleer denemeler veya Çernobil gibi felaketler, genetik mutasyon riskini
artırdı. Örneğin, Körfez Savaşı sonrasında Amerikan askeri personelinde ALS insidansı,
çeşitli çalışmalarda genel popülasyona kıyasla daha yüksek bulunmuştur. Kozmik
ışınlar ise, yüksek irtifada yaşayan popülasyonlarda DNA hasarına yol açmış
olabilir.
Epigenetik faktörler ise genlerin zamanla ifade
mekanizmalarını değiştiriyor. Stres, beslenme veya toksinlere maruz kalma,
genlerin “açılıp kapanmasını” etkiliyor ve bu değişiklikler nesillere
aktarılabiliyor. Mesela, bir atamızın yaşadığı açlık veya zehirli bir ortama
maruz kalması, bugün ALS gibi hastalıkların tetikleyici faktörlerinden biri
olabilir. İnsan zekâsının geliştirdiği teknolojiler de bu denkleme eklendi:
kimyasal maddeler, hava kirliliği ve hatta modern yaşamın stresi, genetik
havuzumuzu ve geleceğimizi şekillendiriyor. Yani, ALS gibi hastalıklar sadece
genetik miras değil, insanlık tarihinin çevresel ve teknolojik serüveninin de
bir yansıması.
ALS ve Dünya
Akrabalığı: Bağlantı Nerede?
ALS’nin genetik hikâyesi, dünya akrabalığıyla kesişiyor. Çünkü
hepimiz ortak bir genetik mirası paylaşıyoruz. Sporadik ALS’de görülen bazı
mutasyonlar, çok eski atalarımızdan miras kalmış olabilir. Bu mutasyonlar,
binlerce yıl boyunca “sessizce” taşındı ve çevresel faktörler, yaşlanma veya
epigenetik değişikliklerle aktif hale geldi. Örneğin, Avrupa’da ALS görülme
oranı 100.000’de 2-3 kişi iken, Pasifik Adaları’nda (ör. Guam) bir dönem çok
daha yüksekti. Bunun nedeni, yerel genetik havuzun daralması ve çevresel
faktörlerin birleşimiydi. Bu örnekler, genetik mirasımızın ve çevrenin
hastalıkları nasıl şekillendirdiğini gösteriyor.
Peki, Ne Yapabiliriz?
ALS’nin genetik şifrelerini çözmek, tedavi umutlarını artırıyor.
Genetik tarama, ailesel ALS riski taşıyanlar için önemli bir araç. Örneğin,
C9orf72 mutasyonu taşıyıcıları erken tespit edilirse, ilerideki tedavilere
hazırlanabilir. CRISPR gibi gen düzenleme teknolojileri ise umut vadediyor.
2023’te, SOD1 mutasyonuna bağlı ALS için bir gen terapisi denemesi başarılı
sonuçlar verdi. Bu, sporadik ALS için de kapıları açabilir. Ayrıca, çevresel
faktörlerin etkisini azaltmak için toksinlere maruziyeti azaltmak, sağlıklı
yaşam tarzını teşvik etmek önemli.
Ama bilim kadar, farkındalık da önemli. ALS, nadir bir
hastalık olsa da, hepimizi birleştiren bir insanlık hikâyesi. Ortak
atalarımızdan gelen genetik miras, hem hastalıkların hem de umudun bir parçası.
Göç yolları, salgınlar ve çevresel faktörler, genetik havuzumuzu şekillendirdi;
şimdi sıra, bu mirası anlamakta ve geleceği iyileştirmekte. ALS hastalarına
destek olmak, araştırmalara katkıda bulunmak veya sadece bu hastalığı anlamak
için bir adım atmak, hepimizin ortak mirasına sahip çıkmak demek.
Son Söz: Birlikte
Daha Güçlüyüz
ALS, genetik ve çevresel bir hastalık olarak korkutucu
görünebilir, ama insanlık tarihi bize bir şey öğretiyor: Hepimiz bağlantılıyız.
Afrika’dan başlayan yolculuğumuz, salgınlar, göçler ve çevresel mücadelelerle
genlerimizde saklı. ALS gibi hastalıklar, bu ortak mirasın bir parçası; ama
aynı zamanda, bu mirası anlamak ve iyileştirmek için bir fırsat. Belki bir gün,
genetik biliminin ve dayanışmanın ışığında, ALS’yi tarihe gömeceğiz. O zamana
kadar, her birimizin hikâyesi, bu büyük insanlık ailesinin bir parçası olmaya
devam edecek.
Dr. Alper Kaya
10 Temmuz 2025