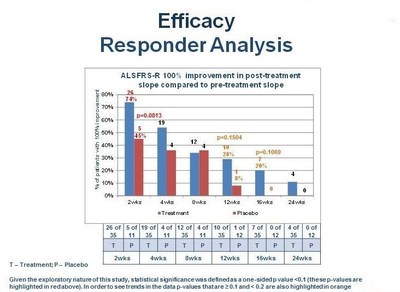
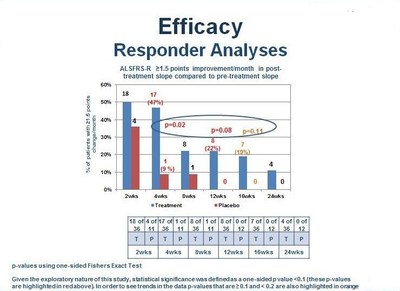
Nöraltus İlaç firması, ALS hastalığında Faz 2 NP001 Çalışmasından elde edilen Sonuçları açıkladı
26 Nisan 2018 - Nörodejeneratif hastalıklar için yenilikçi terapiler geliştirmeye adanmış özel bir ilaç firması olan Neuraltus Pharmaceuticals, Inc., bugün, sistemik inflamatuar özelliği olan ALS hastalarında, NP001 araştırmasının Faz 2 çalışmasından elde edilen bulguları açıkladı.
138 hastayı içeren çalışma, birincil veya ikincil sonlanım noktasını, ALS İşlevsel Derecelendirme Ölçeği-Revize (ALSFRS-R) skorundaki başlangıç değerinde ve FVC değerinde bir değişiklik görülmedi. Top-line veriler, Amerikan Nöroloji Akademisi'nin Los Angeles'taki 26. Yıllık Toplantısı'nda 26 Nisan 2017 günü saat 8: 00'de bir podyum sunumu sırasında sunulacak.
Kaynak:
Yasal Uyarı
Bu site, ALS hastalığı ile ilgili haber ve bilgilendirme sitesidir. Tıbbi tavsiye, teşhis veya tedavi yerine geçmez. Tıbbi bir durumla ilgili sorularınız için her zaman doktorunuzla görüşün.
Dr. Alper Kaya
faz II etiketine sahip kayıtlar gösteriliyor. Tüm kayıtları göster
faz II etiketine sahip kayıtlar gösteriliyor. Tüm kayıtları göster
27 Nisan 2018 Cuma
19 Temmuz 2016 Salı
Brainstorm NurOwn® ABD Faz 2 Çalışması Olumlu Sonuçlarını Açıkladı
Brainstorm NurOwn® ABD Amiyotrofik Lateral Skleroz (ALS) Hastalarında Faz 2 Çalışması Olumlu Sonuçlarını Açıkladı
NurOwn®, kullanılan yöntemin güvenli ve iyi tolere edilebilir olduğunu gösterdi.
Nörodejeneratif hastalıklar için önde gelen yetişkin kök hücre tedavisi geliştiricisi BrainStorm Cell Therapeutics Inc., bugün Amiyotrofik Lateral Skleroz (ALS) Hastalarında Faz 2 çalışmasının sonuçlarını açıkladı. Amerika Birleşik Devletlerinde son zamanlarda ALS Hastalarında plasebo NurOwn® karşı kontrollü, randomize, çift kör kök hücre çalışması tamamlandı. Faz 2 denemesi, 48 ALS hastasında NurOwn güvenliğini ve etkinliğini değerlendirmek için tasarlanmış rasgele, çift kör, plasebo-kontrollü, çok merkezli bir çalışma oldu. çalışma, Amerika'da Massachusetts General Hospital, UMass Medical School ve Mayo Clinic merkezlerinde 24 hafta boyunca yürütüldü. Hastaların kendi kemik iliğinden (autologous bone marrow) alınan hücreler, NurOwn® teknolojisi ile zenginleştirilip hastalara kas içi enjeksiyon ve intratekal (beyin omurilik sıvısına) yolla veriliyor.
Çalışma NurOwn güvenli ve iyi tolere olduğunu göstererek açıkça klinik olarak anlamlı bir fayda gösteren birçok ikincil etkinlik parametrelerine ulaştı. Yanıt oranları, plasebo ile karşılaştırıldığında NurOwn kullanılan yöntemin güvenli ve iyi tolere edilebilir olduğunu gösterdi.
http://www.prnewswire.com/news-releases/brainstorm-announces-positive-top-line-results-from-the-us-phase-2-study-of-nurown-in-patients-with-amyotrophic-lateral-sclerosis-als-300299813.html
21 Nisan 2015 Salı
NP001 İÇİN FAZII KLİNİK DENEMELERİ OLASI YARARLARINI GÖSTERİYOR
Neuraltus Pharmaceuticals Initiates Confirmatory Phase 2 Study of NP001 in Patients with Amyotrophic Lateral Sclerosis
http://www.neuraltus.com/september-22-2016
NP001 faz II sonuçları yayınladı (20 Nisan 2015)
http://www.neuraltus.com/pages/news_rel04_20_15.html
Deneysel ilaç NP001’in denemelerinde ALS’nin ilerleyişini yavaşlattığı ve bazı hastalarda hastalığın ilerleyişinin durduğu saptandı. Faz III aşaması 2013 yılı için planlandı.
Makalenin Özeti :
• NP001, 136 hastada yapılan Faz II aşamasında güvenli bulundu ve iyi tolere edildi.
• Sonuçlar, altı aylık deneme sırasında ilerlemenin yavaşladığı veya durduğunu gösterdi.
• Neuraltus İlaç, 2013 yılında NP001 için Faz 3 çalışmasını başlatmayı ümit ediyor.
Amyotrofik Lateral Skleroz (ALS) olan kişilerde NP001 ilaç denemesinin ikinci aşaması da tamamlandı. Sonuçlar, ilacın bazı katılımcılarda hastalığın ilerleyişini yavaşlatma veya durdurmada etkili olduğunu göstermektedir. Deneyin Baş Araştırmacısı Robert Miller bu sonuçları net bir klinik faydaya çevirmek istediğini belirtti.
Küçük ilaç molekülü NP001, merkezi sinir sistemi içinde kanda ve mikroglia’da bulunan makrofaj adı verilen bağışıklık sistemi hücrelerini hedef alıyor ve aktif saldırı modundan koruma moduna geçmeyi sağlıyor. Araştırmacılar NP001’in etkililiğine baktıklarında, plasebo grubuna kıyasla tedavi grubunda hastalığın ilerleyişi analizinin sonuçları, NP001’in olumlu etkileri ile yüksek doz alımı arasında bir bağlantı olduğunu saptamışlar. Altı aylık bir tedavi döneminde kilogram başına 2mg’lık doz almış olanların yüzde 27 düzeyinde hastalığın ilerleyişi azaldı. Eş zamanlı plasebo grubunda hastalığın ilerlemesi bundan 2,5 kat daha fazlaydı.
ALS MNH Derneği
http://www.neuraltus.com/september-22-2016
NP001 faz II sonuçları yayınladı (20 Nisan 2015)
http://www.neuraltus.com/pages/news_rel04_20_15.html
Deneysel ilaç NP001’in denemelerinde ALS’nin ilerleyişini yavaşlattığı ve bazı hastalarda hastalığın ilerleyişinin durduğu saptandı. Faz III aşaması 2013 yılı için planlandı.
Makalenin Özeti :
• NP001, 136 hastada yapılan Faz II aşamasında güvenli bulundu ve iyi tolere edildi.
• Sonuçlar, altı aylık deneme sırasında ilerlemenin yavaşladığı veya durduğunu gösterdi.
• Neuraltus İlaç, 2013 yılında NP001 için Faz 3 çalışmasını başlatmayı ümit ediyor.
Amyotrofik Lateral Skleroz (ALS) olan kişilerde NP001 ilaç denemesinin ikinci aşaması da tamamlandı. Sonuçlar, ilacın bazı katılımcılarda hastalığın ilerleyişini yavaşlatma veya durdurmada etkili olduğunu göstermektedir. Deneyin Baş Araştırmacısı Robert Miller bu sonuçları net bir klinik faydaya çevirmek istediğini belirtti.
Küçük ilaç molekülü NP001, merkezi sinir sistemi içinde kanda ve mikroglia’da bulunan makrofaj adı verilen bağışıklık sistemi hücrelerini hedef alıyor ve aktif saldırı modundan koruma moduna geçmeyi sağlıyor. Araştırmacılar NP001’in etkililiğine baktıklarında, plasebo grubuna kıyasla tedavi grubunda hastalığın ilerleyişi analizinin sonuçları, NP001’in olumlu etkileri ile yüksek doz alımı arasında bir bağlantı olduğunu saptamışlar. Altı aylık bir tedavi döneminde kilogram başına 2mg’lık doz almış olanların yüzde 27 düzeyinde hastalığın ilerleyişi azaldı. Eş zamanlı plasebo grubunda hastalığın ilerlemesi bundan 2,5 kat daha fazlaydı.
ALS MNH Derneği
6 Haziran 2014 Cuma
Joint Congress of European Neurology - 1 Haziran 2014, İstanbul
EFNS-ENS Joint Congress of European Neurology, Istanbul 2014
Istanbul, Turkey, May 31-June 3, 2014
http://efns2014.efns.org/
Istanbul, Turkey, May 31-June 3, 2014
http://efns2014.efns.org/
Prof. Dr. Nazlı
Başak’ın Sunumu
Türkiye’deki ALS hastalığının belirgin genetik yapısı
hakkında bilgi verdi. Son günlerde Türkiye’de ALS gen mutasyonunun birçok
nüfusta kapsamlı olarak araştırıldığını, toplam 411 Türk ALS hastaları üzerinde
yapılan çalışmada, bunlardan 66 ailede 96 fALS ve sALS vakalarındaki yaygın gen
mutasyonu üzerinde çalışıldığını belirtti. Hastalardan SOD1 VE UBQLN2 gen
mutasyonları için PCR yoluyla genetik özelliklerine göre bir grup
oluşturulduğunu, C9orf72 PP-PCR için hastaların alt kümesi de ayrıca ekzon
dizilemeyle karşı karşıya getirilmiş olduğunu ve SOD1-D906 mutasyonu taşıyan
hastalara haplotip analizinin uygulandığını açıkladı.
Sonuç: SOD(12%), c9ORF72(%13.5) ve UBQ2N2 (%6) Türkiye’de
gen mutasyonları Türkiye’de yaklaşık olarak %30 f ALS hastasına denk
gelmektedir. Buna karşın şu an Türkiye’deki s ALS hastalarında hiçbir SOD1
mutasyonu bulunamamıştır; C9orf72 (%3.5)
ve UBQLN2(%0.7) mutasyonları yapılan kohort çalışmada s ALS hastalığının
%42’sini oluşturmaktadır. Ekzon dizilimi, 4 ailede FUS, OPTN,SPG11 ve PLEKHG5
mutasyonlarını ortaya çıkarmıştır. Daha çok dominant ve çekinik pedigrilerde
ortaya çıkan SOD1-D90A mutasyonları bu tip çalışmada, 3 Türk ailesinde çekinik
karakter olarak görülmüştür.
Prof.Dr. Dimitrios
Karussis’in Sunumu
Kemik İliğinde Bulunan, Kendini Yenileme ve Farklılaşma
Yeteneğine Sahip Yetişkin İnsan Kök
Hücreleri (MSC) ile Tedavi Edilen ALS Hastalarının Analizi: Faz I /II ve
II A Klinik Deneme
Prof. Karussis, bu çalışmanın amacını, altyapısını,
kullanılan metodu ve sonucu hakkında bilgi verdi.
Amaç: ALS hastalarındaki nörotrofik faktörlerin (“MSC-NTF”) salgılanması için MSC hücreleri
ile yapılan tedavinin güvenirliliğini ve tolere edilebilirliğini değerlendirmek
Altyapı: Uygulanan gruba yapılan çalışma, değiştirilmemiş
MSC hücrelerinin, IV/IT uygulamasıyla güvenilir olduğunu göstermiştir.
MSC-NTF’nin nöroptotektif etkileri ALS gibi nörodejeneratif hastalıklarda
çeşitli hayvan modellerinde ispatlanmıştır. Şu an 2 art arda olan klinik
denemelerin ikincisi , bu hücrelerin ALS hastalarında güvenirliliğini ve tolere
edilebilirliğini değerlendirmek için gerçekleştirilmektedir.
Metodlar: MSC hücreleri Brainstorm’un Nur Own teknolojisi
kullanılarak hastanın omuriliğinden alınmaktadır. Bu hücreler dışarıda
çoğaltılarak, GDNF ve BDNF gibi nörotrofik faktörlerin salgılanması için
uyarılmaktadır. Bu Otolog MSC-NTF hücreleri IM veya IT enjeksiyonları ile ALS
hastalarına nakledilmektedir. Bütün hastalar, aylık olarak tedavi öncesi 3 ay
ve nakil sonrası 6 ay izlenmektedir.
Sonuç: Kök hücre nakledilmiş hastaların 6 aylık izleniminde,
tedavi ile ilgili ciddi hiçbir yan etki gözlemlenmemiştir. Klinik izlem
sonucunda Klinik Değişim Oranında (ALSFRS) ve IT ile tedavi edilen hastaların 6
ay sonra solunum fonksiyonlarında (FVC) olumlu değişiklik ortaya çıkmıştır. Bu
klinik deneme, intratekal veya kas içi MSC-NTF enjeksiyonunun güvenilir
olduğunu, kliniksel yararlı etkilerin bazı belirtilerini ortaya çıkarmıştır. Bu
çalışmada görülen güvenilir ve ön etkinlik sonuçları Brainstorm’un daha önceki
Faz I/II deneme sonuçları ile birbirini tutmaktadır. Bu iki çalışma toplam 26 ALS hastası
Brainstorm’un kök hüce tedavisi görmüştür.
Prof. Karussis, şu an yapılan Faz II a denemesinde olan 14
hastadan ilk 10 hasta için analiz sonuçlarını sundu. Sonraki 4 hastanın analiz
sonuçları ise 6 aylık izlenimlerinden sonra verileceğini belirtti.
Hastaların %71 ‘inde tedaviden önceki 3 ay dönem içerisinde
nörolojik fonksiyonlarında zayıflama görüldüğünü; buna karşın, İntratekal veya
birleştirilmiş (IT) ve kas içi (IM) uygulaması ile tedavi olan hastaların
%63’nde, yenilenmiş ALS Fonksiyonel Oran sonuçları ölçülerek, stabilizasyon
veya nörolojik fonksiyonlarında düzelme görülmüştür. Dr Karussis, ön analizdeki
bu farklılıkların istatiksel olarak p=0.335,ki-kare testinde önemli olduğunu
söyledi.
Buna ek olarak, Prof. Karussis, denemenin her iki fazında da
,IT veya birleştirilmiş IT ve IM uygulama yoluyla tedavi edilen hastaların %63’nün, tedaviden 3
ay içinde ALSFRS-R sonuçlarına ve FVC solunum fonksiyon testlerine
bakılarak, tedaviye cevap vermekte
olduğunu belirtmiştir. Daha önce sadece IM yoluyla Nur Own teknolojisi ile
tedavi edilen 6 hastada özellilkle lokal pozitif etki görüldüğünü; aynı şekilde,
aynı Faz I/II denemesinde, IT ile nakledilmiş hastalarda tedavi edilen kolda
CMAP sonuçları ile ispatlanarak nörotrofik ve yenileyici etkilerinin
gözlemlendiğini söyledi. Son olarak da , Nur Own uygulamasının hem kas içinden,
hem de intratekal olarak iyi tolere edildiğini, birçok hastada gözlenen
iyileşme ve stabilizasyonun onu çok cesaretlendirdiğini ve Amerika’da birkaç
merkezde kurulmakta olan yeni çalışmalar için de umutlu olduğunu vurguladı.
Yasemin Akarsu
10 Eylül 2013 Salı
Neuralstem Faz II başladı
Amerika’da Neuralstem Kök kücre Çalışmasında Faz II aşamasında : ilk ALS hastasını ameliyat ettiler.
Türkçesi: Dünyada ALS hastalığının tedavisi/yavaşlatılması için Kök hücre uygulamalar deneme aşamasında devam ediyor. İlk kez FDA onaylı çalışmayı başlatan merkez Emory ALS Center, geçen yıl 12 ALS hastasında Kök hücre Faz1 çalışmasını tamamladı ve bilimsel sonuçları yayınladı. Yapılan çalışmada Kök hücrenin ALS hastaları üzerinde kısa vadede (1 yıl) zararlı etkisi olmadığını, hastalar tarafından tolore edildiği bildirildi. Neuralstem firması ve Michigan Üniversitesi Emory ALS Center işbirliği ile yapılan çalışma, Dr Eva Feldman tarafından yönetiliyor. Ameliyatlar ise Dr Nicholas Boulis tarafından yapılıyor.
Faz 1 aşamasını başarıyla tamamlanan çalışmaya FDA tarafından faz 2 izni verildi. Bu aşamada ALS hastalığında kök hücre uygulamasının hastalığın ilerlemesi üzerinde etkili olup olmadığı araştırılacak. Faz 4 aşamasına kadar henüz kök hücrenin bir ilaç olarak rutin kullanılması mümkün değil. Dünyada tüm ilaçlar aynı aşamalardan geçiyor.
Dünyada ALS hastaları için kök hücre çalışmaları yapan ve FDA protokolu uygulayan diğer birkaç merkezler ver. Onlar da faz 2 aşamasına yeni başlıyorlar.
Türkiye’de böyle bir çalışma henüz yok.
Not: Bu çalışmaları yapan merkezlerin hasta kabul ederken çok sıkı kriterleri var. Hastaları genellikle birkaç seans uygulama yaptıkları için ve ortaya çıkacak beklenmeyen problemlere hazırlıklı olmak için merkezlere yakın, kontrollere gelebilecek ve sağlık sigortalarının herşey dahil ödeme yapanlardan seçiyorlar.
Prensip olarak, bunların dışında hasta almıyorlar.
https://umclinicalstudies.org/HUM00072488
http://clinicaltrials.gov/ct2/show/NCT01730716
Türkçesi: Dünyada ALS hastalığının tedavisi/yavaşlatılması için Kök hücre uygulamalar deneme aşamasında devam ediyor. İlk kez FDA onaylı çalışmayı başlatan merkez Emory ALS Center, geçen yıl 12 ALS hastasında Kök hücre Faz1 çalışmasını tamamladı ve bilimsel sonuçları yayınladı. Yapılan çalışmada Kök hücrenin ALS hastaları üzerinde kısa vadede (1 yıl) zararlı etkisi olmadığını, hastalar tarafından tolore edildiği bildirildi. Neuralstem firması ve Michigan Üniversitesi Emory ALS Center işbirliği ile yapılan çalışma, Dr Eva Feldman tarafından yönetiliyor. Ameliyatlar ise Dr Nicholas Boulis tarafından yapılıyor.
Faz 1 aşamasını başarıyla tamamlanan çalışmaya FDA tarafından faz 2 izni verildi. Bu aşamada ALS hastalığında kök hücre uygulamasının hastalığın ilerlemesi üzerinde etkili olup olmadığı araştırılacak. Faz 4 aşamasına kadar henüz kök hücrenin bir ilaç olarak rutin kullanılması mümkün değil. Dünyada tüm ilaçlar aynı aşamalardan geçiyor.
Dünyada ALS hastaları için kök hücre çalışmaları yapan ve FDA protokolu uygulayan diğer birkaç merkezler ver. Onlar da faz 2 aşamasına yeni başlıyorlar.
Türkiye’de böyle bir çalışma henüz yok.
Not: Bu çalışmaları yapan merkezlerin hasta kabul ederken çok sıkı kriterleri var. Hastaları genellikle birkaç seans uygulama yaptıkları için ve ortaya çıkacak beklenmeyen problemlere hazırlıklı olmak için merkezlere yakın, kontrollere gelebilecek ve sağlık sigortalarının herşey dahil ödeme yapanlardan seçiyorlar.
Prensip olarak, bunların dışında hasta almıyorlar.
http://clinicaltrials.gov/ct2/show/NCT01730716
1 Temmuz 2013 Pazartesi
Genervon GM604 FazII A başlıyor
FDA Tarafından ALS gibi yetim hastalıklarda ilaç araştırmaları yapan firmalara bazı önceliker sağlanıyor. FDA, Genervon firmasına Çalışmasının bir an önce başlatılması için FazII b izni verildi. Buna fast track desteği deniyor.
http://www.clinicaltrials.gov/ct2/show/NCT01854294
İlaç, hastalarda muhtemel bozulmuş gen ifadelerini modere etmek için kullanılıyor.
Temmuz 2013 de Amerika'da 12 ALS hastası çalışmaya alınacak. Temmuz 2014 de FazII A sonuçlarının açıklanması bekleniyor.
http://www.genervon.com/genervon/about_pressreleases.php
Ocak 2015
Fda onayı için bir ALS hastasının başlattığı dilekçe kampanyasını buradan imzalayabilirsiniz
http://www.clinicaltrials.gov/ct2/show/NCT01854294
İlaç, hastalarda muhtemel bozulmuş gen ifadelerini modere etmek için kullanılıyor.
Temmuz 2013 de Amerika'da 12 ALS hastası çalışmaya alınacak. Temmuz 2014 de FazII A sonuçlarının açıklanması bekleniyor.
http://www.genervon.com/genervon/about_pressreleases.php
Ocak 2015
Fda onayı için bir ALS hastasının başlattığı dilekçe kampanyasını buradan imzalayabilirsiniz
Kaydol:
Kayıtlar (Atom)