Yasal Uyarı
28 Aralık 2024 Cumartesi
ALSUntangled #77: Psilocybin
ALSUntangled, hasta ilgisiyle gündeme gelen alternatif ve etiket dışı tedavileri inceliyor. Burada, mantarlardan türetilen ve psikedelikler olarak bilinen ilaç kategorisine ait bir kimyasal olan psilocybin'i inceliyoruz. Psilocybin, kan beyin bariyerini geçme ve nörogenez ve inflamasyona etki etme yeteneği nedeniyle ALS ilerlemesini yavaşlatmak için makul mekanizmalara sahiptir. Şu anda, hastalığı değiştiren tedavi bağlamında psilocybin ve ALS için klinik öncesi ALS modelleri, vaka raporları veya denemeler bulunmamaktadır. Doza bağlı olarak, halüsinasyonlar ve fiziksel zarar gibi yüksek bir psikolojik yan etki riski olabilir. Yukarıdaki bilgilere dayanarak, şu anda ALS ilerlemesini yavaşlatmak için bir araç olarak psilocybin kullanımını desteklemiyoruz.
27 Aralık 2024 Cuma
Yeni Yıl Mesajı: Bir Yılın Ardından
Son yıllarda, genellikle geçen yılı ve önümüzdeki yılı
düşünmek için zaman ayırıyorum. Gözlerim
bilgisayar sanal klavyesinin üzerinde, düşüncelerimi buraya yazıyorum. Tabii
ki, bu her zaman böyle değildi; bilgisayarların olmadığı bir dönemde büyüdüm.
Şimdi böyle bir teknolojiye sahip olduğum için çok şanslıyım ve mutluyum. Bu
teknolojilerin Türkiye’de yaygınlaşması için yazmaya devam edeceğim.
Ancak bu yıl, her zamankinden daha fazla, tekrar kalem ve kâğıda
dönmek istiyorum. Divit, mürekkep
hokkası ve dolmakalem zamanlarını hatırlıyorum. Yazmak, düşünmek ve
hissetmek, varsayılan bedensel
varlığımla daha uyumlu bir eylem gibi geliyor. Yavaşlamak, anı daha
derinlemesine hissetmek… İşte tam da bu anlarda, yılın bu dönemi, beni hep
somut olanla bağlantıya çağırıyor. Fiziksel olarak alışageldiğim 30 yıllık bir
deneyimden sonra sanal ortamda varoluş, insanın sabrı bulabilmesi yolculuğunda
ne kadar değerli olabileceğini hatırlatıyor.
Son yıllarda sabrın bizlerden ne kadar uzak olduğunu
hissediyorum. Belki de teknoloji, her ne
kadar farklı vaatlerde bulunsa da bizi hızla bir yere sürüklüyor ve her geçen
gün birbirimizden biraz daha uzaklaştırıyor.
Birkaç gün önce, 21 Aralık kış dönümü, diğer adıyla Yelda
gününde en uzun gece uykuya dalmadan önce gözlerimi kapattığımda bana
hatırlattığı şey, zamanın uzun olduğu ve bizlerin çağlar boyu gelip
geçtiğimizdi. Ama basit güzellikler her zaman etrafımızda var; çoğu zaman
doğada ya da sevdiklerimle birlikte bunu daha yoğun hissediyorum.
Bizi, bize hatırlatan zamanın fısıldadığı mesajı
hissediyorum:
·
Kibir değil, alçakgönüllülük;
·
Nefret değil, uyum (*) (*) Ostinato, kanada
yapımı kısa animasyon filminde bir besteci, uyumsuz bir sesle mücadele etmek
yerine onu besteye dâhil etmenin beklenmedik derecede güzel bir harmoni
yarattığını fark eder.
·
Zulüm değil, iyilik
Ve her şeyden önce, her insana saygıdır.
Bu belirsiz zamanlarda, belki de her zamankinden daha fazla,
kendimizi başkalarına verebilmeliyiz, ne zaman ve nerede olursa olsun. Empati
ve diğerkâmlık insan olmanın erdemleridir.
Bu, en büyük hediyedir.
Küçük bir jest bile çok değerli olabilir; bir gülümseme
bile. Bazen karanlıkta ışık arayan bir ruh için ne kadar değerli ve takdir
edilebilir olacaktır. Tabii ki, daha
fazla imkânı olanlar için, yapılacak çok daha fazlası vardır ve bizim yaşlı ve
karşılık beklemeden dönüp duran dünyamızın geleceği buna bağlıdır
Bu yıl dünyada ALS hastalığı ile mücadele yolunda kayda
değer gelişmelere şahit olduk. Başarısız girişimlerden çok önemli dersler
alındı. Geri adım atmak yerine üzerine daha birikimli gitmeyi öğrendik. Aralık ayında Montreal’de yapılan yıllık
ittifak toplantısı, profesyoneller forumu ve ALS/MND sempozyumuna sanal olarak
katıldık. Yılın sonunda ALS hastalığı karşısında küresel bir işbirliği ve
küresel bir bakış açısı geliştiğine tanık olduk. ALS-MNH Derneği olarak
uluslararası platformda ülkemizi temsil ettik. Türk Nöroloji Derneği
Nöromüsküler Hastalıklar ve yaşam kalitesi çalışma gruplarında yer aldık.
Çeşitli kamu kurumları ile irtibat kurduk. Ambulansta hasta yakını alınması
konusuna açıklık getirdik. SOD1 mutasyonlu ailesel ALS hastalarında Qalsody
(Tofersen) ilacı ile ilgili olarak
girişimler devam ediyor. Yurtdışından getirilebilecek ilaçlar listesine alındı.
SGK kapsamında ödenmesi için gerekli başvurular yapıldı. Antalya Şubemiz evde
hemşire ziyaretleri programımız tamamlandı. İstanbul ve İzmir’de aynı program
2016 yılından beri devam ediyor. İstanbul Maratonunda Yardımseverlik koşusunda
toplanan bağışlar ile proje kapsamında cihaz ve malzeme desteği devam ediyor.
Şubat ayında koşucularımıza ve bağışçılarımıza teşekkür amacıyla bir tören
düzenliyoruz. Yakında duyurulacak. Ses bankası projemiz ile ilgili olarak bizi
izlemeye devam ediniz. Dijital dönüşüm
projemiz kabul edildi. Sivil toplum destek vakfı ile çalışıyoruz.
Bu yılki çalışmalarımızda, katılabilenlere ve
katılamayanlara, hepinizin kalbimizde olduğunuzu, şükran ve sevgiyle
hatırladığımızı belirtmek isterim.
2024 sonrasında size en içten dileklerimizi gönderiyor, 2025
için en iyi dileklerle sağlık ve huzur dolu bir yıl geçirmenizi temenni
ediyoruz.
(*) Ostinato, kanada yapımı kısa animasyon filminde bir
besteci, uyumsuz bir sesle mücadele etmek yerine onu besteye dâhil etmenin
beklenmedik derecede güzel bir harmoni yarattığını fark eder.
ALS'de kilo kaybından önce beslenme tüpü takılması en iyi seçenektir
Tanı ve PEG arasındaki kilo kaybının sağ kalımı etkilediği görülmektedir.
Yapılan bir araştırmaya göre, çok fazla kilo verdikten sonra beslenme tüpü takılan amiyotrofik lateral skleroz (ALS) hastalarının, büyük kilo kaybından önce beslenme desteği alanlara göre birkaç ay içinde ölme olasılıkları daha yüksek.
Araştırmacılar, bulguların, önemli kilo kaybından önce yerleştirilen beslenme tüplerinin ALS hastalarının yaşam süresini uzatabileceğini gösterdiğini söyledi.
Beslenme tüpleri, ALS hastalarının hastalık ilerledikçe beslenme ihtiyaçlarına yardımcı olur
ALS, motor nöron hastalığı veya MND olarak da adlandırılır, ilerleyici kas güçsüzlüğü ile belirginleşen bir rahatsızlıktır. Hastalık ilerledikçe, hastalar genellikle yiyecekleri etkili bir şekilde çiğneme ve yutma yeteneklerini kaybederler .
Çoğu durumda, karın duvarından mideye bir tüp yerleştirilerek gıdanın doğrudan sindirim sistemine iletilmesinin sağlandığı cerrahi bir işlem olan gastrostomi yapılması tavsiye edilir.
Gastrostomi, ALS'li kişilerin artık yiyecek yiyemedikleri zaman beslenme ihtiyaçlarını karşılamalarına yardımcı olarak hayat kurtarıcı bir önlem olabilir. Ancak bilim insanları, gastrostominin ne zaman yapılması gerektiğine dair net bir kılavuz olmadığını belirtti.
Gastrostomi sonrası erken ölüm oranını öngören faktörleri belirlemek için Avustralyalı bir bilim insanları ekibi, 2015 ile 2021 yılları arasında Perth'deki bir hastanede bu prosedüre tabi tutulan 94 ALS hastasının sonuçlarını analiz etti. Hastalığın teşhisinden gastrostomiye kadar geçen ortalama süre yaklaşık sekiz ay (227 gün) idi.
Araştırmacılar, beslenme tüpü yerleştirilmesinden sonraki 30, 90 ve 180. günlerde ölüm riskinin artmasıyla ilişkili değişkenleri araştıran istatistiksel testler yürüttüler.
Daha zayıf akciğer fonksiyonu ve yaşlılık gibi bazı faktörler, bazı zaman noktalarında artan ölüm riskiyle ilişkilendirilirken, diğerlerinde ilişkilendirilmedi. Ancak analiz edilen tüm zaman noktalarında, sonuçlar tutarlı bir şekilde gastrostomi geçirmeden önce daha fazla kilo vermiş hastalarda ölüm riskinin daha yüksek olduğunu gösterdi.
Editör beslenme tüplerini 'destekleyici müdahale' olarak görüyor, ancak kişisel bir karar
Araştırmacılar, "Verilerimiz, 90 ve 180. günlerdeki ölüm oranının, tanıdan gastrostomiye kadar geçen süredeki kilo kaybı yüzdesinden etkilendiğini tutarlı bir şekilde gösteriyor ve bu da MND popülasyonunda beslenme bakımının önemini vurguluyor" diye yazdı.
Bilim insanları, bulguların "Önemli kilo kaybından önce gastrostomi yerleştirilmesinin kilo kaybına bağlı ölüm riskini azaltabileceğini" öne sürdüğünü belirterek, bu fikrin kesin olarak test edilmesi için daha fazla çalışmaya ihtiyaç duyulduğunu vurguladı.
Çalışmayla birlikte yayınlanan bir başyazıda , bu bulguların, beslenme tüpü takılmasının çiğneme ve yutma güçlüğü çeken hastalar için yalnızca destekleyici bir önlemden daha fazlası olabileceğini vurguladığı belirtiliyor; yeterli beslenmeyi sağlamak için zamanında yapılan müdahale, ALS hastalığının seyrini etkileyebilir.
Nebraska Tıp Merkezi Üniversitesi'nde nörolog olan Dr. Gary L. Pattee, "Gastrostomi artık hastalığın gidişatını olumlu yönde etkileyen aktif destekleyici müdahalenin bir yolu olarak düşünülmelidir" diye yazdı. "Hastalık sürecinin erken dönemlerinde ideal vücut ağırlığını korumanın önemi, artık birçok klinik çalışmada uzun süreli hasta sağ kalımı elde etmede elzem olarak kabul edilmiştir."
Bu sonuçlar gastronomi biliminin potansiyel faydalarını ortaya koyarken, Pattee beslenme tüpü takılmasının önemli bir karar olduğunu ve hastaların isteklerinin önceliklendirilmesi gerektiğini vurguladı.
"Gastrostomi, tıbbi ekip, hasta ve bakıcılar arasında paylaşılan karar almayı gerektiren, hastanın nihai isteklerine her zaman saygılı olunması gereken önemli bir klinik ve kişisel karardır" diye yazdı.
20 Aralık 2024 Cuma
2024 March of Faces
16 Aralık 2024 Pazartesi
Danny Reviers; 45 yıllık bir mücadele sonunda aramızdan ayrıldı.
https://turkals.blogspot.com/2022/04/danny-reviers-ve-mia-mahynin-hikayesi.html
14 Aralık 2024 Cumartesi
Masitinib (masitinib mesilat) pazarlama izninin reddedilmesi Hk
Pazarlama izni neden reddedildi?
İlk değerlendirme sırasında EMA, EMA ve diğer düzenleyici otoriteler tarafından koordine edilen İyi Klinik Uygulama (GCP) denetimlerinden elde edilen bulguların, çalışmanın yürütülmesiyle ilgili yeterince ele alınamayan sorunları tespit etmesi nedeniyle çalışma verilerinin güvenilir olmadığını değerlendirdi. Ayrıca Masitinib AB Science'ın faydaları ikna edici bir şekilde kanıtlanamadı; çalışma, genel çalışma popülasyonu için temel etkililik ölçüsünde ilaç ve plasebo arasında hiçbir fark bulamadı ve birkaç metodolojik soruna sahipti. Sağlanan verilerin yeniden incelenmesinden ve bir grup nöroloji uzmanı ve hasta temsilcisiyle istişarede bulunulduktan sonra bu endişeler değişmedi. Ajans, nihai kararını verirken hasta kuruluşları tarafından sağlanan bilgileri de (üçüncü taraf müdahaleleri olarak adlandırılan) dikkate aldı. Bu nedenle Ajans, Masitinib AB Science'ın faydalarının risklerden daha ağır basmadığı yönündeki tutumunu korudu ve pazarlama izninin reddedilmesini tavsiye etti.
Şirket, Masitinib AB Science'ın klinik denemelerinde hastalar üzerinde herhangi bir etkisinin bulunmadığı konusunda Ajans'ı bilgilendirdi.
10 Aralık 2024 Salı
Ibudilast (Ketas) hk
Ketas (Ibudilast) : Faz IIb/III (COMBAT-ALS) çalışması devam eden Ibudilast (Mn-166) etken maddesini içeriyor. İbudilast henüz ALS hastalığı için FDA onayı almamıştır. Yurtdışında Piyasada Online satılıyor. Onaylı olmadığı için eczanelerde ve Türkiye’de bulunmuyor. Çalışma devam etmektedir.
Aralık 2024
Amiyotrofik lateral skleroz (ALS) için araştırma amaçlı bir oral tedavi olan MN-166 (ibudilast), devam etmekte olan Faz 2b/3 klinik çalışmasındaki verilerin analizine göre, bir yıla kadar kullanımda hastalığın ilerlemesini yavaşlatıyor gibi görünüyor. Çalışmanın tasarımı kapsamında gerekli olan ara analiz, altı aylık tedavide standart hastalık ilerlemesi ölçümlerindeki bulguların altı ay sonrasına kadar bildirilenlerle ne kadar iyi korelasyon gösterdiğine baktı. Çalışmanın veri güvenliği izleme kurulu (DSMB) verileri inceleyip onayladı ve COMBAT-ALS (NCT04057898) çalışmasının planlandığı gibi devam etmesini tavsiye etti. Tedavinin geliştiricisi MediciNova'nın baş tıbbi sorumlusu ve direktörü Kazuko Matsuda, MD, PhD, bir şirket basın açıklamasında "Bu sonuçların ALS gibi hızla ilerleyen hastalıklar için çalışmalar tasarlamada değerli olacağına inanıyoruz" dedi
Matsuda, "Tedavi süresinde bir değişiklik yapmayı düşündük, [ancak] DSMB'nin tavsiyesine dayanarak denemeye mevcut tedavi planıyla devam etmeye karar verdik" diye ekledi.
Analiz sonuçları, 6-8 Aralık tarihlerinde Montreal'de düzenlenen 35. Uluslararası ALS/MND Sempozyumu'nda sunuldu. Sunumun başlığı "ALS'de MN-166 (Ibudilast) COMBAT-ALS Faz 2b/3 Denemesi: Deneme Güncellemesi ve Ara Analiz Sonuçları" (sayfa 242) başlığını taşıyordu.
https://www.tandfonline.com/doi/pdf/10.1080/21678421.2024.2403306 (Sayfa 242)
7 Aralık 2024 Cumartesi
5 Aralık 2024 Perşembe
ALS-MNH Derneği 23. Yılını kutluyor!
Değerli ALS-MNH Derneği Üyeleri, Destekçileri ve Sevgili Dostlar,
Bugün, ALS-MNH Derneği'nin 23. kuruluş yıldönümünü gurur ve mutlulukla kutluyoruz. Yola çıkarken küçük bir ışıkla başlayan bu serüven, azimle, sevgiyle ve dayanışma ruhuyla büyüdü. Birlikte geçirdiğimiz bu uzun yıllar, engelleri aşmanın, umut olmanın ve bir arada güçlü durmanın hikayesidir.
23 yıl önce, futbolun zirvesindeyken ALS ile tanışan iki futbolcu, İsmail Gökçek ve Sedat Balkanlı’nın öncülüğünde kurulan derneğimiz, bugün binlerce insanın hayatına dokunmuş, umut olmuş ve toplumsal farkındalık yaratmıştır. Bu yolda birlikte yürüdüğümüz hasta ve hasta yakınlarına, gönüllülere, bağışçılara ve destekçilere minnettarız. Sizlerle birlikte bu başarıları elde etmek, geleceğe daha umutla bakmak bize güç veriyor.
Her birinizin, bu derneğin başarılı bir sivil toplum örgütü olmasına katkıda bulunan birer kahraman olduğunu düşünüyoruz. Geçtiğimiz 23 yıl boyunca kaybettiğimiz dostlarımıza rahmet diliyoruz ve onların hatırasını yaşatmaya devam edeceğiz.
Bu kutlu gün vesilesiyle, ALS-MNH Derneği olarak bir gün ALS'ın olmadığı bir dünyaya ulaşma hayalimize inanan tüm dostlarımıza teşekkür ediyoruz. Birlikte daha nice yıllara, daha güçlü ve umut dolu projelere yürümeyi diliyoruz
Saygılarımızla,
ALS/MNH Derneği
Yönetim Kurulu Adına
Başkan Dr. Alper KAYA
19 Kasım 2024 Salı
European medicine agency (EMA), ALS tedavisi için NUZ-001'e (monepantel) yetim tıbbi ürün statüsü verilmesini önerdi
Avrupa İlaç Ajansı (EMA), amyotrofik lateral skleroz (ALS) tedavisi için NUZ-001'e (monepantel) yetim tıbbi ürün statüsü verilmesini önerdi. Aralık ayında Avrupa Komisyonu tarafından nihai onayı beklenmesi beklenen bu statü, Neurizon Therapeutics'e düzenleyici ücretlerin azaltılması, deneme protokollerinde yardım ve onay üzerine 10 yıllık pazar ayrıcalığı gibi avantajlar sağlayacaktır. Başlangıçta bir veteriner solucan ilacı olan NUZ-001, sinir hücrelerini korumaya ve ALS ile ilişkili toksik protein birikimlerini temizlemeye yardımcı olabilecek mTOR sinyal yolunu engelleme potansiyeli nedeniyle ALS için yeniden kullanılıyor. 12 ALS hastasını içeren bir Faz 1 denemesi (NCT04894240), NUZ-001'in ALS Fonksiyonel Derecelendirme Ölçeği-Revize (ALSFRS-R) ile ölçüldüğü gibi hastalığın ilerlemesini yavaşlatabileceğini gösterdi. Terapi ayrıca bu yılın başlarında ABD'de yetim ilaç statüsü aldı.
18 Kasım 2024 Pazartesi
ALS yol haritası tercih Kılavuzu
ALS tedavi seçenekleriniz hakkında bilgi edinmek ve bakımınızla ilgili önemli kararlar almak için My ALS Decision Tool™'u kullanabilirsiniz. Örneğin, hastalığınız ilerledikçe, ALS bakım ekibiniz mümkün olduğunca sağlıklı ve rahat kalmanıza yardımcı olmak için solunum desteği veya beslenme tüpü gibi tedaviler önerebilir. Şu anda kendi başınıza nefes almakta veya yemek yemekte sorun yaşamıyor olsanız bile, gelecekteki bakımınız için planlama yapmaya başlamak için asla erken değildir. Her modülde ilerlerken, bazı yaygın ALS tedavileri ve prosedürleri hakkında bilgi edinecek, sizin için neyin en önemli olduğunu düşünmenize yardımcı olacak birkaç soruyu yanıtlayacak ve ALS bakım ekibinizle seçenekleriniz hakkında konuşmaya hazır olacaksınız.
https://lesturnerals.org/my-als-decision-tool/
7 Kasım 2024 Perşembe
Ekstraselüler vezikül tedavisi: Ekzosom
Ekstraselüler vezikül tedavisi: Ekzosom
Kök hücre tedavileri
deneyseldir!
3.10.2024
Mezenkimal kök hücre konusunda Brainstorm firması çok
çalışıyorlar. Nurown teknolojisi kullanılıyor. Hastadan alınan kemik iliğinden
Nurown teknolojisi il kök hücre zenginleştiriliyor. ALS hastalığında İntratekal
enjeksiyon (Beyin omurilik sıvısı içine) şeklinde uygulanıyor. Fakat henüz ALS
hastalığında elde edilen sonuçlar FDA tarafından yetersiz bulunmaktadır.
Mayo klinikte yağ dokusu kaynaklı kök hücreler FazII
çalışmasında belirgin bir yavaşlama göstermedi. Mayo Clinic'te nöroloji
profesörü olan Nathan P. Staff, MD, PhD, "ALS'de Tekrarlanan İntratekal
Otolog Adipoz Türevli MSC'lerin Faz 2 Klinik Çalışmasının Sonuçları"
başlıklı konuşmasında, "Genel kohortta güçlü bir etkinlik sinyali
görmedik, ancak katılımcıların bir alt kümesine bakıldığında yanıt veren bir
etki olabilir" dedi."
Uygulamaya bağlı yan etkiler ve bağışıklık sistemi
etkileşimi ile ilgili komplikasyonları dışında zararsız olduğu bildiriliyor.
Bugüne kadar amiyotrofik lateral skleroz için etkili bir
tedavi bulunmamaktadır. Bu bağlamda, amiyotrofik lateral sklerozu iyileştirmek
için eksozomların, mezenkimal kök hücrelerin ve nörotrofik faktörlerin
kullanımına ilişkin araştırmalar bilim camiasında büyük ilgi görmektedir.
Mezenkimal kök hücreler bağışıklık yanıtını modüle eder,
oksidatif stresi azaltır, nöronal rejenerasyonu destekler ve nöronal ve glial
hücrelere farklılaşır. Ayrıca, mezenkimal kök hücrelerden elde edilen eksozomlar,
mezenkimal kök hücrelerin anormal farklılaşmasını önleyerek ana hücreleri
üzerinde faydalı etkiler gösterir. Benzer şekilde, nörotrofik faktörler
enflamatuar yanıtı düzenler, nöron onarımını ve nöronal fonksiyonların
iyileşmesini uyarır. Bu nedenle, nörotrofik faktörlerle birleştirilmiş otolog
mezenkimal kök hücre türevli eksozomlar, amiyotrofik lateral skleroz için
potansiyel olarak etkili bir girişimsel ortam olabilir.
https://www.sciencedirect.com/science/article/abs/pii/S094096022200036X
https://www.mdpi.com/2075-1729/13/1/121
Extracellular vesicle
therapy: Exosome
Hücrelerden izole edilen hücre dışı veziküller (EV'ler) de
benzer potansiyele sahiptir.
Çeşitli içerikler (protein, mikroRNA, vb.) farklı roller
oynamaktadır.
Araştırmalar ayrıca endotel hücreleri, astrositler ve motor
nöron benzeri hücreler gibi çeşitli hücre hedeflerini de araştırmıştır.
ALS ile ilişkili patolojik proteinler ve nükleotitler, prion benzeri bir şekilde yayılmak için EV'leri kullanır.
Amiyotrofik lateral
sklerozda hücre dışı veziküllerin terapötik ve tanısal potansiyeli
Üst ve alt motor nöronları etkileyen geç başlangıçlı ve ölümcül bir nörodejeneratif hastalık olan amiyotrofik lateral skleroz (ALS), patogenez mekanizmaları üzerinde daha fazla araştırma yapılmasını gerektiren, teşhis ve tedavisi zor bir hastalıktır. Buna ek olarak, merkezi sinir sistemindeki (MSS) hastalıkla ilgili hücreleri hedef almak için kan beyin bariyerini (BBB) geçerek terapötiklerin iletilmesindeki zorluklar nedeniyle, ALS gibi hastalıkların yönetimi özellikle zordur. Bununla birlikte, nanotıp alanındaki son gelişmeler yeni fırsatlar sunmuştur. Hücre dışı veziküller (EV'ler) küçük, küresel, nano boyutlu partiküller olup, doğal özellikleri ve ilaç taşıma kabiliyetleri sayesinde ALS'nin tedavi ve teşhisinde çeşitli uygulanabilir özellikler göstermiştir. Köken hücreler tarafından belirlenen benzersiz kargolara sahip hücre dışı veziküller nöral koruyucu niteliklere sahiptir ve BBB'yi geçebilir ve endojen ve/veya tasarlanmış kargoyu belirli nöral hücre hedeflerine iletebilir. Bu derlemede, EV'lerin ALS için terapötikler, ilaç dağıtım sistemleri ve biyobelirteçler olarak potansiyel kullanımını hala tartışmalıdır.
Amiyotrofik lateral sklerozda hücre dışı veziküller (Eksosom) Rutin ve
onaylı bir yöntem olarak henüz kabul edilmiyor.
https://onlinelibrary.wiley.com/doi/full/10.1002/nep3.26
25 Ekim 2024 Cuma
Japonya'da ALS için Vitamin B12 tedavisi Rozebalamin onaylandı
Doğal olarak oluşan bir B12 vitamini formu olan mekobalaminin ultra yüksek dozu, Japonya'da amiyotrofik lateral sklerozu (ALS) tedavi etmek için Rozebalamin marka adı altında onaylandı
Eisai tarafından üretilip pazarlanacak olan tedavinin , hastalığa sahip kişilerdeki işlevsel gerilemeyi yavaşlatması amaçlanıyor.
Eylül ayındaki onay , Rozebalamin'in tek başına veya standart ALS tedavileriyle birlikte verildiğinde ALS hastalığının ilerlemesini önemli ölçüde yavaşlattığını gösteren JETALS (NCT03548311) adlı bir Faz 3 klinik çalışmasından elde edilen verilere dayanıyordu .
Şirket bir basın bülteninde , "Eisai, ALS hastaları için yeni bir tedavi seçeneği olarak Rozebalamin sağlayarak hastaların ve ailelerinin çeşitli ihtiyaçlarını daha da karşılamaya ve faydalarını artırmaya kararlıdır" dedi .
Mecobalamin ışığa karşı oldukça hassastır ve bu da kimyasal olarak dengesiz hale gelmesine neden olabilir. Şirket, boyun kısmında sağlık çalışanlarının seyreltme ve geri çekme sırasında ilacı kolayca görmelerini sağlayan yeniden kapatılabilir bir pencere bulunan yüksek düzeyde ışık koruması sağlayan bir şişe yarattı. Ayrı bir şirket basın bültenine göre, Japan Institute of Design Promotion ambalaja İyi Tasarım Ödülü'nü verdi .
Masitinib hakkında olumsuz görüş
Avrupa İlaç Ajansı'ndan (EMA) oluşan bir danışma komitesi, AB Science'ın masitinib ilacına Avrupa Birliği'nde amiyotrofik lateral skleroz (ALS) için oral ek tedavi olarak koşullu pazarlama izni verilmesine karşı görüşünü onadı
Karar, şirketin masitinib hakkındaki ilk olumsuz görüşün yeniden incelenmesini istemesinin ardından bu ay İnsan Kullanımına Yönelik Tıbbi Ürünler Komitesi'nin (CHMP) düzenlediği toplantıda alındı
AB Science'ın kurucu ortağı ve CEO'su Alain Moussy, bir şirket basın bülteninde " EMA incelemesinin bir parçası olarak yeniden muayene sürecini destekleyen hastalara ve doktorlara minnettarız. Tüm bu çabaları hastalar için yaptık" dedi .
AB Science ayrıca , düzenleyici kurumunun Şubat ayında masitinib'i koşullu olarak onaylamamaya karar verdiği Kanada'da yeniden değerlendirme için başvuruda bulundu . Ancak şirket, Sağlık Kanada'nın yeni gönderilen analizleri mevcut verilerin yeni analizleri olarak değil, yeni veriler olarak değerlendirmesinin ardından yeniden değerlendirmeye devam etmemeye karar verdi. Bu, kurumun yönergelerine göre yeniden değerlendirme sürecinde izin verilmeyen bir durumdur. Sağlık Kanada, çözülmemiş sorunları ele almak için yeni bir başvuru gönderme seçeneği sunarak terapi için olası bir ilerleme yolu gösterdi.
Masitinib, bağışıklık hücrelerinin inflamatuar bir yanıt oluşturması için moleküler ipuçlarını aktive eden tirozin kinaz adı verilen bir enzim türünün inhibitörüdür.
1 Ekim 2024 Salı
Kök hücre tedavisi, Faz 2 denemesindeki herkes için ilerlemeyi değiştirmedi
AAN 2024: (Amerikan Nöroloji Derneği)
ALS için kök hücre tedavisi bazı hastalarda hastalığı yavaşlatıyor Ancak MSC'lerle tedavi, Faz 2 denemesindeki herkes için ilerlemeyi değiştirmedi
Faz 2 klinik çalışmasından elde edilen yeni verilere göre, kök hücre tedavisi, özellikle mezenkimal kök hücreler veya MSC'lerle tedavi, amiyotrofik lateral skleroz (ALS) hastalarında hastalığın ilerlemesini önemli ölçüde değiştirmedi. Bununla birlikte, tedaviden kayda değer faydalar sağladığı görülen bir hasta alt kümesi vardı ve ALS için kök hücre tedavisinden sonra ilk MSC enjeksiyonunu almadan öncesine göre en az %25 daha yavaş ilerledi.
Mayo Clinic'te nöroloji profesörü olan Nathan P. Staff, MD, PhD, "ALS'de Tekrarlanan İntratekal Otolog Adipoz Türevli MSC'lerin Faz 2 Klinik Çalışmasının Sonuçları" başlıklı konuşmasında, "Genel kohortta güçlü bir etkinlik sinyali görmedik, ancak katılımcıların bir alt kümesine bakıldığında yanıt veren bir etki olabilir" dedi."
https://www.aan.com/msa/Public/Events/AbstractDetails/5559
Mezenkimal kök hücrelerin kullanımı araştırma amaçlı olarak kabul edilir, yani Gıda ve İlaç Dairesi (FDA) tarafından rutin klinik kullanım için onaylanmamıştır. Ancak FDA bu araştırma çalışmasında mezenkimal kök hücrelerin kullanımına izin vermiştir.
https://clinicaltrials.gov/study/NCT03268603#study-overview
Mezenkimal kök hücrelerin kullanımı araştırma amaçlı olarak kabul edilir, yani Gıda ve İlaç Dairesi (FDA) tarafından rutin klinik kullanım için onaylanmamıştır. Ancak FDA bu araştırma çalışmasında mezenkimal kök hücrelerin kullanımına izin vermiştir.
11 Eylül 2024 Çarşamba
Yavaşlamak
Zaman esnektir, ancak nihayetinde sınırlı ve değeri bilinmeyen bir kaynaktır. İnsanlar bu gerçeği, haberlerde yer alan trajediler ya da ara sıra yaşadıkları sağlık sorunları aracılığıyla kısa süreliğine hatırlar ve ardından çılgın yaşamlarına geri dönerler. ALS hastaları için zaman anlayışımız evrim geçiriyor. ALS her ne kadar işleri yavaşlatan bir hastalık olsa da, ailemize zamanımızı bireysel olarak ve birlikte nasıl kullandığımızı yeniden düşünme fırsatı veriyor. Önceliklerimizi yeniden belirlemeyi, bilinçli kararlar almayı ve değerli olduğunu hissettiğimiz şeylere odaklanmayı öğreniyoruz. ALS zamanımızı elimizden almadı, aksine zamanımızı nasıl harcadığımızı yeniden değerlendirmeye sevk etti.
Slowing Down—A Family’s Experience With ALS
Andrea M. Shamaskin-Garroway, PhD, Joel Shamaskin, MD: JAMA
Neurol. 2024;81(9):907-908. doi:10.1001/jamaneurol.2024.1922
2 Eylül 2024 Pazartesi
NE ZAMAN TRAKEOSTOMİ YAPILMALIDIR?
Solunum yetmezliği bulguları başladığında Bipap adı verilen solunum cihazı ve maske ile solunum desteği verilirse trakeostomi yapılması geciktirilebilir. Ancak ağız içi tükürük salgısının aşırı artışı nedeniyle solunum yolları temiz tutulamıyor ve yutma güçlüğü başladıysa maske ile solunum cihazı desteği riskli olabilir. Bu durumda trakeostomi en mantıklı çözümdür.
Ayrıca, yetersiz ve zayıf öksürük nedeniyle balgam atılamıyor ve sık sık solunum yolu enfeksiyonu yaşanıyorsa trakeostomi gerekebilir.
Eğer hasta solunum sorunları nedeniyle yoğun bakıma yatırılmış ve bu dönemde solunum desteği hava yoluna konan bir tüp aracılığı ile sağlanmış ve bu süre 15 günü geçmişse ve bu süre içerisinde solunum cihazından ayrılması mümkün olamamışsa bu kez hastanın soluk borusuna cerrahi bir işlemle “trakeostomi” açılır ve “trakeostomi kanülü” konulur.
Trakeostomi neden gerekir?
Eğer Non-invaziv ventilasyon (solutma) uzun sürerse ağız bakımı zorlaşır ve maskenin temas ettiği yerlerde yaralar oluşur. Hastaya ağız bakımı yetersiz olursa, ağıc içinde üreyen mikroplar kolayca akciğere inerek iyileşme süresini uzatacak yeni enfeksiyonlara sebep olabilirler.
Solunum güçlüğü ortaya çıktığında, kan oksijenini ve karbondioksit ölçülerek trakeostomi kararı verilebilir. Trakeostomi, ALS hastalarında balgam ve tükürük yoğunluğu olan hastaların öksürme refleksleri ve yutkunma refleksleri azaldığı ya da bittiğinde yapılması gerekir. Hastanın tükürüğünün akciğerlere kaçmasını önlenmek ve gelen balgamı aspire edilebilmek için soluk borusuna ufak bir delik açılır. Bu delik ilk başta solunum makinesine bağlanmayacaksa gümüş kanül, silikon veya plastik kanül kullanılabilir. Hasta solunum makinesine bağlanacak ise balonlu (cuff) plastik kanül takılır.
Açılan delikte, soluk borusu ve bronşlarda biriken balgam aspire makinesi ile çekilir ve hasta rahatlatılır. Aynı şekilde yutkunma sorunu olduğu için ağızda biriken tükürük aspire makinesi yardımı ile hastaya sıkıntı vermeden temizlenebilir.
Bu tür hastalarda kas güçsüzlüğü olduğu için dilin sırt üstü yatma durumlarında boğaza kaçma olasılığı çok yüksektir. Yatakta sürekli sağ kol ya da sol kol üstüne yatıldığında hastada kemik ağrıları olmaktadır. Bu durumda hastalar, havalı yatak ile çok rahat ederler.
ALS hastalarında erken açılan trakeostomi ile hastada nefes alma sırasında rahatlama görülmektedir. Boğulma-zatürre riski azalır. Nefes almada rahatlama, balgam sorununun aspirasyon ile temizliği gibi birçok faydası bulunmaktadır.
Eğer hastanın konuşması bozuk ise trakeostomi yapıldığında hastadan ses gelmemektedir. Fakat konuşma normal ise trakeostomi yapıldığında da konuşma mümkün olmaktadır. Konuşma yeteneği zamanla kaybedilebilir. Henüz anlaşılabilir şekilde konuşabilen hastalarda ses bankası, ses klonlama imkanı mevcuttur. Trakeostomi ses tellerine zarar vermeden gerçekleştirilen bir operasyondur.
Trakeostomi operasyonları hastanede yapılan kısa süreli bir operasyondur.
Ayrıca aşağıdaki adrese gözatın
Balgam sorunu
Hastam balgam çıkaramıyor
Ne zaman Ventilator (solunum cihazı) ?
27 Ağustos 2024 Salı
ANKET DUYURUSU (Ses klonlama)
ANKET DUYURUSU
Eğer sesimi ve konuşmamı kaybedecek olursam gelecekte kendi sesimi kullanabilir miyim?
Ses klonlama tekniği ile sesinizi gelecekte kullanabilmek artık mümkün.
Aşağıdaki anket ses klonlama hakkında bir ön çalışmadır.
Kendi sesinizle iletişim kurabilmek için ön başvuru yapabilirsiniz.
16 Ağustos 2024 Cuma
Kaliforniya Üniversitesi’ndeki bilim insanları çığır açıcı bir beyin çipi geliştirdi.
Brain gate grubu Amerika'da birkaç merkezde 2009 yılında başlatılan bir proje. Toplam 28 uygun hasta çalışmaya alınacak. Girişimsel bir yöntem. Beynin korteks bölgesine elektrot yerleştiriliyor. Kelimeler bir ekranda görülüyor. Uygun bir metin okuyucu yazılımla uzun süreli etkilerinin değerlendirilmesi gerekiyor. 2038 yılında tamamlanması bekleniyor.
ALS nedeniyle 7 yıldır sesini
kaybeden bir adam, yapay zeka kullanarak sesini geri kazandı. Eski videolardan
sesini klonladı ve beyin sinyallerini konuşmaya dönüştürdü.
15 Ağustos 2024 (HealthDay News)
-- Casey Harrell, Lou Gehrig hastalığı olarak da bilinen amiyotrofik lateral
skleroz (ALS) nedeniyle konuşma yeteneğini kaybediyordu.
"İletişim kuramamak çok
sinir bozucu ve moral bozucu. Sanki kapana kısılmışsınız gibi," diyor 45
yaşındaki Harrell.
Ancak yeni bir beyin-bilgisayar
arayüzü, Harrell'in bir kez daha başkalarıyla konuşmasına olanak tanıyor; beyni
sözcükleri sağlarken, bilgisayar da onlara ses veriyor.
Konuşmayı koordine etmekten
sorumlu beyin bölgesine yerleştirilen dört mikroelektrot dizisi, Harrell'in
söylemek istediği kelimeleri tespit ediyor ve bu bilgiyi bir bilgisayar
programına gönderiyor.
Araştırmacılar, Harrell'in ilk
seansında sistemin 50 kelimelik bir kelime dağarcığıyla yüzde 90'ın üzerinde
kelime doğruluğuna ulaşmasının 30 dakika sürdüğünü söyledi.
Çözümlenen kelimeler bir ekrana
yansıtılıyor ve Harrell'in ALS hastalığına yakalanmadan önceki sesine benzeyen
bir sesle yüksek sesle okunuyor.
"Sistemi ilk denediğimizde,
doğru bir şekilde söylemeye çalıştığı kelimeler ekranda belirince sevinçten
ağladı. Hepimiz öyle yaptık," dedi araştırmacı Sergey Stavisky ,
Kaliforniya Üniversitesi, Davis Nöroprostetik Laboratuvarı eş direktörü.
Araştırmacılar, ALS'nin vücuttaki
hareketi kontrol eden sinir hücrelerini etkilediğini söyledi. Ayakta durma,
yürüme, elleri kullanma ve hatta konuşma yeteneğinin kademeli olarak
kaybolmasına neden oluyor.
Harrell çalışma odasına
girdiğinde kollarında ve bacaklarında güçsüzlük oluşmuştu ve konuşması çok zor
anlaşılıyordu.
Temmuz 2023'te araştırmacılar,
Harrell'in beynine elektrotlar yerleştirerek konuşmayla ilgili beyin aktivitesini
kaydedebildiler.
Stavisky, üniversitenin bir basın
bülteninde, "Kaslarını hareket ettirme ve konuşma girişimlerini gerçekten
tespit ediyoruz," diye açıkladı. "Bu komutları kaslara göndermeye
çalışan beynin bir kısmından kayıt yapıyoruz. Ve temel olarak bunu dinliyoruz
ve bu beyin aktivitesi kalıplarını bir foneme -- bir hece veya konuşma birimi
gibi -- ve sonra da söylemeye çalıştıkları kelimelere çeviriyoruz."
Araştırmacılar,
bu tür beyin-bilgisayar arayüzlerinin (BCI) geliştirilmesinin
önündeki engellerden birinin, bilgisayarın beyin sinyallerini doğru
şekilde nasıl yorumlayacağını öğrenmesinin zaman alması olduğunu söyledi.
“Önceki konuşma BCI sistemlerinde
sık sık kelime hataları oluyordu. Bu, kullanıcının tutarlı bir şekilde
anlaşılmasını zorlaştırıyordu ve iletişimin önünde bir engel oluşturuyordu,”
diyor araştırmacı Dr.
David Brandman , UC Davis'te nöroşirürji
yardımcı doçenti. “Amacımız, birinin konuşmak istediği her an anlaşılmasını
sağlayacak bir sistem geliştirmekti.”
Araştırmacılar, Harrell'in
cihazla yaptığı ikinci seansta potansiyel kelime dağarcığının 50'den 125.000
kelimeye çıktığını tespit etti.
Sadece 1,4 saatlik ek eğitim
verisiyle BCI, büyük ölçüde genişletilmiş kelime dağarcığının yanı sıra %90'lık
bir kelime doğruluğuna ulaştı.
Harrell'in
vakasıyla ilgili bir rapor 14 Ağustos'ta New England Journal of Medicine'de yayımlandı .
Araştırmacılar, Harrell'in 32
hafta boyunca 248 saatten fazla iletişim kurduğu 84 veri oturumunun ardından
sistemin artık %97'den daha iyi bir doğruluk oranına sahip olduğunu söyledi.
Brandman, "Bu noktada,
Casey'nin söylemeye çalıştığı şeyi %97 oranında doğru bir şekilde
çözebiliyoruz. Bu, bir kişinin sesini yorumlamaya çalışan birçok ticari akıllı
telefon uygulamasından daha iyi" dedi.
Brandman, "Bu teknoloji
dönüştürücüdür çünkü konuşmak isteyen ancak konuşamayan insanlara umut
sağlar," diye ekledi. "Bu konuşma BCI gibi teknolojilerin gelecekteki
hastaların aileleri ve arkadaşlarıyla konuşmalarına yardımcı olmasını
umuyorum."
Harrell da aynı fikirde.
"Böyle bir teknoloji
insanların hayata ve topluma dönmesine yardımcı olacak" dedi.
https://www.nejm.org/doi/full/10.1056/NEJMoa2314132
https://clinicaltrials.gov/study/NCT00912041#participation-criteria
https://x.com/i/status/1826055324069146876
10 Ağustos 2024 Cumartesi
Erkeklerde idrar yolu enfeksiyonu en sık nedeni
Prostat büyümesi
İdrar sondası
Az sıvı alımı
Diyabet
Prezervatif sonda:
Ucuz sondalar yara yapabilir
idrar torbası hortumu ciltte tahriş alerji yapabilir
Bulabildiğim en iyi sonda ve idrar torbası Coloplast conveen
En küçük ölçü ile deneyin, çift taraflı yapıştırıcı bant gerek kalmaz. Bant alerji yapabilir.
Gündüz kullanın gece çıkarın.
Pahalı ama rahat.
Prostat büyümesi
Prostat büyümesi varsa idrar yapma hissi geldiğinde zor idrar yapma oluyor. Böyle bir durum varsa Üroloji uzmanı ilaç yazıyor idrar çıkışı rahat oluyor.
İdrar sondası
Foley sonda olarak bilinir. Silikon olanları tercih edin.
Plastik ördek kullanmak da enfeksiyon riskini arttırıyor. cam kavanoz temizliği daha kolay
Günde 1500 cc en az sıvı almaya gayret edin
9 Ağustos 2024 Cuma
FUS - Amyotrofik Lateral Skleroz | ION363
FUS Mutasyonlu Amyotrofik Lateral Skleroz Katılımcılarında ION363'ün Etkinliğini, Güvenliğini, Farmakokinetiğini ve Farmakodinamiğini Değerlendirme Çalışması (FUS-ALS)
Bu çalışmanın birincil amacı, amiyotrofik lateral sklerozlu (FUS-ALS) sarkom mutasyonlarında kaynaşmış taşıyıcılarda ION363'ün klinik fonksiyon ve sağkalım üzerindeki etkinliğini değerlendirmektir.
95 katılımcıdan oluşan çok merkezli, üç bölümlü bir çalışmasıdır. Bölüm 1, 60 haftalık bir süre boyunca çok dozlu ION363 veya plasebo rejimi almak üzere 2:1 oranında randomize edilecek katılımcılardan oluşacak, ardından katılımcıların 84 haftalık bir süre boyunca açık etiketli ION363 alacağı Bölüm 2 gelecektir. Katılımcılar Bölüm 3'te 3 yıla kadar veya ION363 hastanın ülkesinde ticari olarak mevcut olana kadar veya Sponsor ION363 geliştirme programını sonlandırana kadar (hangisi daha önce gerçekleşirse) açık etiketli ION363 almaya devam edebilirler.
https://clinicaltrials.gov/study/NCT04768972
Çalışma merkezleri aşağıdadır
https://clinicaltrials.gov/study/NCT04768972#contacts-and-locations
İlginenler için https://ionistrials.com/i-am-interested-in-a-study/
ionisNCT04768972study@clinicaltrialmedia.com
Türkiye’de çalışma yoktur.
Bir ALS hastasının sosyal medya hesabı
Jacob Harper, 24, diagnosed with ALS in March, 2022! Fighting for a cure through a clinical trial at Ohio State University! "Genetic FUS-Gene Mutation
https://www.tricals.org/en/trials/fusion-trial/
4 Ağustos 2024 Pazar
Qalsody (Tofersen) konusunda yeni gelişmeler
Daha önce SOD1 mutasyonu taşıyan als hastalarımız için yurtdışından getirilebilecek ilaçlar listesine Qalsody ilacının eklenmesi ve SGK kapsamında temin edilmesi için Nöroloji uzmanı hocalarımız başvuru yapmıştı. Tarih itibariyle ilacın etkinliği kanıtlanmamıştır gerekçesiyle Türkiye İlaç Tıbbi Cihaz Kurumu, talepleri reddetmişti.
Yakın zamanda İsveç’te yapılan ENCALS toplantısında ilacın etkinliğini kanıtlayan çalışmalar sunuldu.
Sonuç olarak;
SOD 1 mutasyonu olan ALS hastaları için FDA, EMA onayı almış olan Qalsody (Tofersen) ilacı, 1 Temmuz 2024 itibariyle Avrupa’da Almanya, Fransa, İsveç, Hollanda, Belçika'da geri ödeme kapsamına alınmıştır.
Ne yazık ki ilaç Türkiye’de yok. Türkiye’de henüz geri ödeme kapsamına alınmadı. İlacı geliştiren Biogen firması henüz ruhsat başvurusunda bulunmadı. Bu süreci hızlandırmak için hastalar olarak talep etmeli ve sosyal medyada görünür olmalıyız.
Bu gelişme üzerine Nöroloji uzmanı hocalarımız yeni kanıtlarla Türkiye İlaç Tıbbi Cihaz kurumuna hastalar için Qalsody ilacının Türkiye’de temini ve SGK kapsamında ödenmesi için tekrar başvuru yaptı.
ALS-MNH Derneği olarak aynı gerekçe ile Türkiye İlaç Tıbbi Cihaz kurumu ve SGK kurumuna başvuru yaptık.
Change org kampanya linki aşağıdadır. Sadece imzalayalım ve paylaşalım. Herhangi bir ücret ödenmesi gerekmiyor. Dileyenler Change org çalışanlarını destekleyebilir. Zorunlu değildir.
İmza ver; SOD1 Mutasyonlu ALS Hastaları Tedavi Olsun!
https://chng.it/CDNPyMq2fT
1 Ağustos 2024 Perşembe
C9orf72 ile ilişkili amyotrofik lateral sklerozlu yetişkinlerde antisens oligonükleotid BIIB078 çalışması durduruldu
C9orf72 ile ilişkili amyotrofik lateral sklerozlu yetişkinlerde antisens oligonükleotid BIIB078'in güvenliği, tolere edilebilirliği ve farmakokinetiği: faz 1, randomize, çift kör, plasebo kontrollü, çoklu artan doz çalışması
C9orf72 genindeki hekzanükleotid tekrar dizisi uzaması, amiyotrofik lateral sklerozun (ALS) yaygın bir genetik nedenidir. C9orf72'yi hedefleyen herhangi bir tedavi mevcut değildir. BIIB078, C9orf72 mRNA'sını hedefleyen araştırma aşamasındaki bir antisens oligonükleottittir. Bu çalışmada, C9orf72 ile ilişkili ALS'li katılımcılarda BIIB078'in güvenliğini, tolere edilebilirliğini ve farmakokinetiğini değerlendirmeyi amaçladık.
Yöntemler
Bu faz 1, randomize kontrollü çalışma altı ülkede (Kanada, İrlanda, Hollanda, İsviçre, İngiltere ve ABD) 22 merkezde gerçekleştirilmiştir. ALS ve C9orf72'de patojenik bir tekrar genişlemesi olan yetişkinler, altı kohort içinde, kohort başına 3:1 oranında İnteraktif Yanıt Teknolojisi aracılığıyla, intratekal bolus enjeksiyon yoluyla BIIB078 (kohort 1-6'da sırasıyla 5 mg, 10 mg, 20 mg, 35 mg, 60 mg veya 90 mg) veya plasebo almak üzere rastgele atanmıştır. Tedavi dönemi, yaklaşık 2 haftada bir uygulanan üç yükleme dozu çalışma tedavisinden ve ardından 1-3. kohortlar için yaklaşık 3 aylık ve 4-6. kohortlar için yaklaşık 6 aylık bir tedavi dönemi boyunca aylık idame dozlarından oluşmuştur. Hastalar ve araştırmacılar tedavi ataması konusunda maskelenmiştir. Birincil sonlanım noktası advers olayların ve ciddi advers olayların insidansıydı. Bu çalışma ClinicalTrials.gov'a (NCT03626012) kaydedilmiştir ve tamamlanmıştır.
Bulgular
10 Eylül 2018 ile 17 Kasım 2021 tarihleri arasında 124 hasta çalışmaya dahil edilmek üzere taranmıştır. 18 hasta çalışma dışı bırakılmış ve 106 katılımcı kaydedilerek 5 mg (n=6), 10 mg (n=9), 20 mg (n=9), 35 mg (n=19), 60 mg (n=18) veya 90 mg (n=18) BIIB078 veya plasebo (n=27) almak üzere rastgele atanmıştır. 106 hastanın 58'i (%55) kadındır. Tüm hastalar en az bir doz çalışma tedavisi almış ve tüm analizlere dahil edilmiştir. Tüm katılımcılar en az bir advers olay (yan etki) yaşamıştır; advers olayların çoğu hafif veya orta şiddette olmuş ve tedavinin kesilmesine yol açmamıştır.
BIIB078 ile tedavi edilen katılımcılarda en sık görülen yan etkiler düşme, prosedürel ağrı, baş ağrısı ve post lomber ponksiyon sendromudur. BIIB078'in herhangi bir dozunu alan 79 hastanın 14'ü (%18) ciddi yan etki) bildirirken, plasebo alan 27 hastanın dokuzu (%33) ciddi advers olay bildirmiştir. BIIB078 alan beş katılımcı ve plasebo alan üç katılımcıda ölümcül yan etki görülmüştür: 10 mg BIIB078 alan bir katılımcıda solunum yetmezliği, 35 mg BIIB078 alan iki katılımcıda ALS kötüleşmesi, 35 mg BIIB078 alan bir katılımcıda travmatik intraserebral hemoraji, 60 mg BIIB078 alan bir katılımcıda pulmoner emboli ve plasebo alan üç katılımcıda solunum yetmezliği. Tüm ölümler raporlayan araştırmacı tarafından çalışma tedavisiyle ilişkili olmadığı şeklinde değerlendirilmiştir.
Yorum
31 Temmuz 2024 Çarşamba
Qalsody (Tofersen) ilacı hakkında
23 Temmuz 2024 Salı
20 Temmuz 2024 Cumartesi
Oturma minderleri hakkında
Oturma Minderleri, sünger, jel ve hava hücreli çeşitleri ile özellikle uzun süreli tekerlekli sandalye kullananlar için üretilmiştir. Omurilik felçliler, omurga eğrilikleri, ağrı duyusu bozukluğu olan hastalarda kullanılıyor.
Fiyatları 5bin-35bin tl arasındadır. Hava hücreli olanlarda hücre yüksekligi, sibop sayısı, allerjik olmaması, en*boy ölçüleri farklıdır.
ALS hastalığında duyu bozukluğu olmaz. Bizler oturduğumuz yerde rahatsız olduğumuzda bunu hissederiz. Minder kullanmak bir süre hareketsiz oturanlarda faydalı olabilir. Fakat ALS hastalığı ilerleyici bir hastalıktır. Tekerlekli sandalyede oturma süresi giderek azalıyor. Ayrıca kaykılma özelliği (tilt) olmayan sandalyede, sırtı yatabilir olsa da öne doğru kayma oluyor. Bu durumda sürekli arkaya çekmek gerekiyor. En iyi minderi de kullansa hasta rahat edemiyor.
Eğer dünya standartlarında Permobil, Quantum gibi bir akülü sandalyeniz varsa ağırlığı hem mindere hem sırt kısmına dağıtan kaykılma (tilt) özelliği varsa havalı oturma minderini daha rahat ve etkili kullanabilirsiniz.
Kısacası hastanın oturabilme süresi ve hastalığın ilerleme durumuna göre değişiyor.
5-8 bin tl size yük olmayacaksa havalı minder deneyebilirsiniz. Bu tür ürünler açıldığında iade edilemiyor.
3 Temmuz 2024 Çarşamba
ALS hastalığı hakkında doğrular ve yanlışlar
Amyotrofik lateral skleroz (ALS), spor yaralanmaları ve kalıtımsal olduğu yönündeki yanlış anlaşılmalar da dahil olmak üzere pek çok yanlış anlaşılmaya yol açan karmaşık bir hastalıktır.
ALS teşhisi konulmuş olsun veya bir bakıcı olun, ALS
gerçeklerini bilmek önemlidir. İşte hastalıkla ilgili bazı yaygın mitler ve her
iddianın gerçeği.
Spor yapmak ALS'ye neden olabilir
ALS, 1939 yılında teşhisi konulan ve bu duruma dikkat çeken
ünlü beyzbol oyuncusu Lou Gehrig'in adıyla da bilinir.
Bu durum, özellikle diğer profesyonel sporculara, özellikle
de futbolculara ALS teşhisi konduktan sonra, spor yapmakla ALS hastalığının
ortaya çıkması arasında bir bağlantı olduğuna dair inancın oluşmasına yardımcı
oldu.
Bazı çalışmalar futbol oynamakla ALS hastalığının gelişmesi
arasında bir bağlantı olduğunu gözlemlemiştir. 1960 ile 2019 yılları arasında
Ulusal Futbol Ligi'nde oynayan 19.000'den fazla erkeği inceleyen bir çalışmaya
göre, bunlardan 38'ine ALS teşhisi konmuş ve 28'i bu durumdan ölmüştür.
Çalışma, profesyonel futbol oynamanın ALS'ye neden olduğunu
göstermese de, ALS'nin daha çok profesyonel veya temas gerektiren sporlar yapan
kişilerde görülen tekrarlayan kafa travmalarından kaynaklanabileceğine dair
mevcut kanıtlara katkıda bulunuyor.
Ancak atletik olmanın veya eğlence amaçlı spor yapmanın ALS
riskini artırdığına dair gerçek bir kanıt yoktur.
ALS bulaşıcıdır
Bazı insanlar ALS hastası olan birinden hastalığın
geçebileceğine inanıyor.
Basitçe söylemek gerekirse, ALS bulaşıcı değildir.
ALS, hasta birine dokunmak veya yakın mesafede bulunmak gibi
sıradan temaslarla kişiden kişiye bulaşmaz; bu, sıradan soğuk algınlığında
olduğu gibidir.
Ancak genetiğinizin ALS geliştirme riskinizi etkilediğine dair
güçlü kanıtlar var. Bir düzineden fazla gendeki mutasyonlar kesin olarak ALS
ile ilişkilendirildi ve çok daha fazla genin potansiyel olarak hastalık
riskiyle ilişkili olduğu gösterildi.
Tanı konulduktan sonra yaşam beklentisi çok kısadır
ALS teşhisi konulduktan sonraki iki ila beş yıl içinde
hayatınızın sona erdiğine dair bir inanış vardır. ALS'nin ilerleyici ve ölümcül
bir nörodejeneratif hastalık olduğu doğru olsa da, teşhisten sonraki sağ kalım
süresi büyük ölçüde değişir.
ALS'li kişilerin yaklaşık %20'si beş yıldan fazla yaşar ve
yaklaşık %10'u 10 yıl veya daha fazla yaşar. Küçük bir yüzdesi onlarca yıl
yaşar, tıpkı teşhisinden sonra 50 yıldan fazla yaşayan ünlü fizikçi Stephen
Hawking'in durumunda olduğu gibi.
Genç kişiler ve başlangıç semptomları kol veya bacak
kaslarını etkileyen uzuv başlangıçlı ALS'si olanlar, ilk önce baş ve boyun
kaslarında güçsüzlük yaşayan bulber başlangıçlı ALS'si olanlara göre daha iyi
bir prognoza sahip olma eğilimindedir. Tıbbi bakımdaki ilerlemeler yaşam
kalitesini iyileştirmiştir ve araştırmalar ve klinik deneyler yeni ALS
tedavileri için umut sunmaktadır.
Lyme hastalığı ALS'ye yol açabilir
ALS'nin Lyme hastalığı nedeniyle ortaya çıktığı düşüncesi,
büyük olasılıkla kas güçsüzlüğü ve yorgunluk gibi bazı benzer nörolojik
semptomlara sahip olmalarına dayanmaktadır.
ALS için bilinen bir tedavi olmasa da, enfekte bir kenenin
ısırmasıyla insanlara bulaşan Lyme hastalığı genellikle antibiyotiklerle etkili
bir şekilde tedavi edilebilir. Ancak ALS'de tedaviler semptomları yönetmeye
odaklanır.
Gençler ALS hastalığına yakalanmaz
ALS'nin sadece ileri yaştaki yetişkinleri etkilediğini
düşünmek yanlıştır.
ALS hastalığı genellikle 55-75 yaş aralığındaki kişilerde
teşhis edilse de genç yetişkinler ve nadir durumlarda gençler ve küçük çocuklar
da dahil olmak üzere her yaşta ortaya çıkabilir.
Bu inanış, ALS belirtileri gösteren genç kişilerde teşhis ve
tedavinin gecikmesine yol açabilir; çünkü sağlık hizmeti sağlayıcıları bunu
başlangıçta başka bir sağlık sorunuyla karıştırabilir.
ALS kalıtsaldır
ALS hastalığının genellikle anne veya babanızdan birinden
veya her ikisinden miras alındığı düşünülür.
ALS vakalarının yaklaşık %10'unda kalıtsal bir bileşenin
bulunduğu doğrudur; bu durumda hastalığa ailesel ALS adı verilir.
Ancak ALS vakalarının büyük çoğunluğu bilinen bir aile
öyküsü olmadan, sporadik olarak ortaya çıkar.
Yine de, sporadik ALS'li kişilerin yaklaşık %10'u bilinen
ALS genlerinde mutasyonlar taşır. Bu nedenle, hem ailevi hem de sporadik ALS
hastalarına en yaygın ALS'ye neden olan mutasyonları kontrol etmek için genetik
test önerilmelidir. Hastalıkla ilişkili bir mutasyonu belirlemek genellikle ALS
tanısını doğrulamak için yeterli değildir, ancak en iyi tedavi yolunu
belirlemeye yardımcı olabilir.
ALS çoğunlukla erkekleri etkiler
ALS hastalığının başlangıçta erkeklerde daha sık görüldüğü
düşünülüyordu ancak yapılan araştırmalar cinsiyet farkının daha önce
düşünülenden daha dar olduğunu gösteriyor.
ALS erkeklerde yaklaşık %20 daha fazla görülse de, erkekler
ve kadınlar arasında tanı oranları yaş ilerledikçe eşitlenme eğilimindedir.
ALS'nin kadın ve erkekleri farklı şekilde etkileyip
etkilemediği, bunun cinsiyetler arasındaki hormonal farklılıklardan mı, yoksa
genetik veya çevresel faktörlerden mi kaynaklandığı konusunda araştırmalar
yapılıyor.
ALS beyninizi etkilemez
ALS hastalığının bedensel olarak sizi güçsüzleştirdiği,
ancak zihninizin ve bilişsel işlevlerinizin hâlâ tam kontrol altında olduğu
yönünde yanlış bir kanı var.
ALS ile ilgili temel gerçeklerden biri, istemli kas
hareketlerini kontrol etmekten sorumlu motor nöronları etkilemesidir. Ancak,
bazı kişilerde biliş ve davranışı da etkileyebilir.
Daha yeni çalışmalar, ALS hastalarının yarısının
hastalıklarının seyri sırasında bir noktada bilişsel veya davranışsal
değişiklikler yaşayacağını göstermektedir. En yaygın değişiklikler, yönetici
işlevlerdeki anormalliklerdir - eylemlerinizi planlama ve kendi davranışınızı
düzenleme yeteneğiniz.
ALS tedavi edilebilir
ALS hastalığının bazı takviyeler alınarak, insülin iğneleri
yapılarak veya taşınabilir nöromodülasyon uyarıcı cihazlar kullanılarak tedavi
edilebileceği söyleniyor.
Benzer şekilde, ALS tedavisiyle ilgili bir diğer inanış da,
ALS semptomlarını bir şekilde iyileştirdiğini iddia eden birini tanıyorsanız,
onun yaptığı her şeyi yapmanız ve aynı sonucu alacağınızdır.
ALS hastalığının şu anda bir tedavisi yoktur.
Ancak, hastalığın ilerlemesini yavaşlatmaya ve sağ kalımı
uzatmaya yardımcı olabilecek onaylı tedaviler vardır. Ayrıca semptomları
yönetmeye ve yaşam kalitenizi iyileştirmeye yardımcı olan ilaçlar ve ilaç dışı
tedaviler de vardır.
ALS için alternatif ve etiket dışı tedaviler hakkında
bilimsel olarak desteklenen bilgiler için, kırmızı şarap içmekten resveratrol
bileşenlerinden bakır takviyeleri almaya kadar her şeye A'dan F'ye veya henüz
bilinmeyenler için U'ya kadar not veren hakemli bir site olan ALS Untangled'ı
inceleyin.
Doğru ALS bilgilerini anlamak, sizin ve ailenizin tedavi ve
bakım hakkında bilinçli kararlar almanıza yardımcı olabilir. ALS sağlık
ekibiniz sizinle tedavi seçeneklerini, günlük bir rutin oluşturmayı,
uyarlanabilir donanım kullanmayı, duygusal iyiliğinize bakmayı ve ALS ile
yaşamanın diğer yönlerini görüşecektir.
Avrupa İlaç Ajansı'nın (EMA) danışma komitesi, masitinib onayına karşı çıkıyor
Avrupa CHMP, masitinib onayına karşı çıkıyor
Avrupa İlaç Ajansı'nın (EMA) danışma komitesi, masitinib'in amiyotrofik lateral skleroz (ALS) tedavisinde oral ek tedavi olarak kullanılmasına koşullu pazarlama izni verilmemesini önerdi.
İnsan Kullanımına Yönelik Tıbbi Ürünler Komitesi'nin (CHMP) olumsuz görüşü , komitenin geçen ay duyurduğu, güvenlik konusunda herhangi bir endişe olmamasına rağmen deneme protokolü ve veri analizleriyle ilgili bir dizi çözülmemiş sorun olduğu görüşünü doğruluyor .
Geliştirici AB Science, yeniden inceleme talep etmeyi planladığını söyledi, ancak bir basın bülteninde "ALS'de koşullu pazarlama yetkisinin zorluğunu" vurguladı ve "bu yeniden incelemenin ardından olumlu bir sonuç garanti edemeyeceğini" söyledi.
Masitinib, bağışıklık hücrelerinin inflamatuar bir yanıt oluşturmasına yardımcı olan bir enzim türü olan tirozin kinazları güçlü bir şekilde inhibe etmek için tasarlanmış küçük bir moleküldür. Bu enzimleri inhibe etmenin, ALS'de inflamasyonu azaltması ve sinir hücrelerini hasardan koruması, hastalığın ilerlemesini yavaşlatması beklenmektedir.
Şirketin başvurusu, ALS hastası 394 yetişkinin katıldığı bir Faz 2/3 klinik çalışma olan AB10015'ten (NCT02588677) alınan verilere dayanıyordu. Deneme, standart ALS ilacı Rilutek'e (riluzol) ek olarak yaklaşık bir yıl boyunca günde iki kez verilen iki doz masitinib'i (3 veya 4,5 mg/kg) bir plaseboya karşı test etti .
Hastalığın ilerlemesi yavaşladı
ALS Fonksiyonel Değerlendirme Ölçeği-Revize (ALSFRS-R) düşüş oranının ayda 1,1 puandan az olduğu normal hastalık ilerlemesi olan bir hasta grubunda, masitinib'in 4,5 mg/kg dozu, plaseboya kıyasla hastalığın ilerlemesini %27 oranında yavaşlatarak çalışmanın ana hedefine ulaşmıştır.
Kombinasyon tedavisi, normal seyir izleyen hastalarda yaşam kalitesi ve akciğer fonksiyonlarında belirgin bir düşüşe yol açarken, hızlı seyir izleyen hastalarda herhangi bir değişiklik gözlenmedi.
Normal ve hızlı ilerleyen hastalar birlikte incelendiğinde, hafif veya orta dereceli ALS'li hastalar en fazla faydayı gördü , iki yıldan fazla yaşadılar ve masitinib ile plaseboya göre %42 daha yavaş ilerlediler.
CHMP, etkinlik verilerini incelerken çalışmanın yürütülme biçiminde ele alınamayan sorunlar tespit etti. Şirket, iyi klinik uygulamayla ilgili endişelerin, standart prosedürlerden sapmaların sonuçları etkilemediğini göstererek ele alındığını söyledi.
CHMP ayrıca, hızlı ilerleyen hastalığı olan hastaların birincil analizden hariç tutulması kararıyla ilgili endişelerini dile getirdi ancak şirket, çalışmanın tamamlanması için daha tutarlı bir popülasyona ihtiyaç duyulduğunu savundu. AB Science, hariç tutmanın çalışmanın kör olduğu sırada yapıldığını ve bu sayede herhangi bir önyargının ortadan kaldırıldığını söyledi.
Danışma komitesi ayrıca hafif veya orta şiddette ALS hastalarının analizlerine de itiraz etti. Şirket, ikna edici bir risk-fayda profiline sahip bir grup belirlemek için EMA'nın post-hoc analizler (çalışma tamamlandıktan ve tüm veriler toplandıktan sonra yürütülenler) için yönergelerini izlediğini söyledi. Şirket ayrıca grubun "önemli bir 12 aylık sağ kalım avantajı da dahil olmak üzere son derece ikna edici sonuçlar gösterdiğini" yazdı.
Şirket ayrıca CHMP tarafından önerilen farklı istatistiksel analizlerin sürekli olarak olumlu sonuçlar gösterdiğini belirterek, eksik verilerin nasıl işlendiğine ilişkin sorunları da ele aldığını söyledi.
https://alsnewstoday.com/news/europe-chmp-recommends-against-masitinib-authorization/
Çin, bilimsel araştırma ekibi, açık kaynaklı, çip üzerinde beyin bilgisayar akıllı etkileşim sistemi geliştiriyor
Son zamanlarda, Tianjin Üniversitesi Beyin-Bilgisayar Etkileşimi ve İnsan-Bilgisayar Entegrasyonu Haihe Laboratuvarı ekibi, Güney Bilim ve Teknoloji Üniversitesi ve diğer ekiplerle birlikte, açık kaynaklı çip üzerinde beyin-bilgisayar arayüzü akıllı etkileşim sistemi olan MetaBOC'yi ortaklaşa geliştirdi. Robotun engellerden kaçınması için "beyni" geliştirme hedefi, takip etme ve kavrama gibi görevlerin insansız kontrolü, beyin benzeri bilgi işlem için çeşitli ilhamları tamamladı. Araştırma sonuçlarından bazıları yakın zamanda beyin bilimi alanında uluslararası bir dergi olan Brain'de yayınlandı.
Çip üzerindeki beyin iki bölüme ayrılmıştır: "çip" (elektrot çipi) ve "beyin" (in vitro kültürlenmiş beyin). Çip üzerinde beyin, insan vücudunun dışında "beyne benzer bir doku" oluşturmak için kök hücre kültürü teknolojisini kullanıyor. Biyolojik beyinlerin bazı akıllı işlevlerine sahiptir ve elektrot çipleriyle donatılmış olup, bilim adamlarının robotta hata ayıklamasına veya engellerden kaçınmak ve nesneleri yakalamak için robotu otonom olarak kontrol etmek gibi belirli işlevleri gerçekleştirmek için dışarıya sinyaller göndermesine olanak tanır.
"Çip üzerinde beyin arayüzü, in vitro kültürlenmiş 'beyinlerin' (beyin organoidleri gibi) elektrot çipleriyle birleştirilmesiyle oluşturulan çip üzerinde beyindir. Haihe Laboratuvarı genel müdürü Ming Dong, Tianjin Üniversitesi Başkan Yardımcısı, Beyin-bilgisayar etkileşimi ve insan-bilgisayar entegrasyonu dedi.
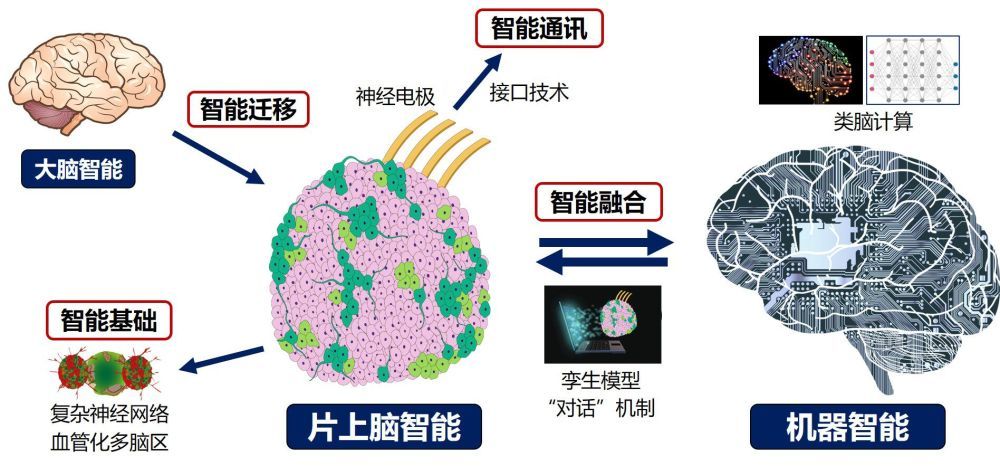
Çip üzerinde beyinle ilgili teknolojilerin temel alanları. (Fotoğraf görüşmeci tarafından sağlanmıştır)

Çip üzerinde beyinin gelecekteki uygulama senaryolarının gösteri diyagramı. (Fotoğraf görüşmeci tarafından sağlanmıştır)
Mingdong, deneysel konular olarak esas olarak insan beynini veya diğer biyolojik beyinleri kullanan geleneksel teknolojilerin aksine, çip üzerinde beyinin beyin-bilgisayar arayüzleri alanında yeni ortaya çıkan önemli bir dal haline geldiğini ve kesme teknolojisinin gelişiminde devrim yaratmasının beklendiğini söyledi. Hibrit zeka ve beyin benzeri hesaplama gibi ileri teknolojik alanlar.
Tianjin Üniversitesi Tıp Fakültesi'nde profesör ve Haihe Beyin-Bilgisayar Etkileşimi ve İnsan-Bilgisayar Entegrasyonu Laboratuvarı'nın çip üstü beyin-bilgisayar arayüzü ekibinin başkanı Li Xiaohong, bu araştırmanın esas olarak iki açıdan çığır açıcı olduğunu söyledi: Birincisi, hücre kültürü iki boyutludan üç boyutluya geçti; çip üzerinde beyin daha karmaşık sinirsel hesaplama ağları sağlıyor. İkincisi, yapay zeka algoritmalarının eklenmesi hibrit zeka alanında girişimlere olanak sağlamıştır.
Buna ek olarak ekip, insan kaynaklı beyin organoitlerinin büyümesi ve gelişmesinde fiziksel alanların rolünü doğruladı, beyni düzenlemek için düşük yoğunluklu odaklanmış ultrasonun prensibini ve mekanizmasını açıkladı ve beyin için daha iyi bir zeka temeli sağladı. çip üzerinde akıllı etkileşim sistemi MetaBOC." beyin".
https://h.xinhuaxmt.com/vh512/share/12076644?d=134d8f3&channel=weixin











